Управління з продовольства та медикаментів США (FDA) одночасно схвалило дві клітинні генні терапії для лікування потенційно смертельної серповидноклітинної анемії у пацієнтів віком від 12 років. Одна з них є і першим схваленим FDA лікуванням, що використовує технологію редагування генів CRISPR/Cas9, повідомляє американський регулятор.
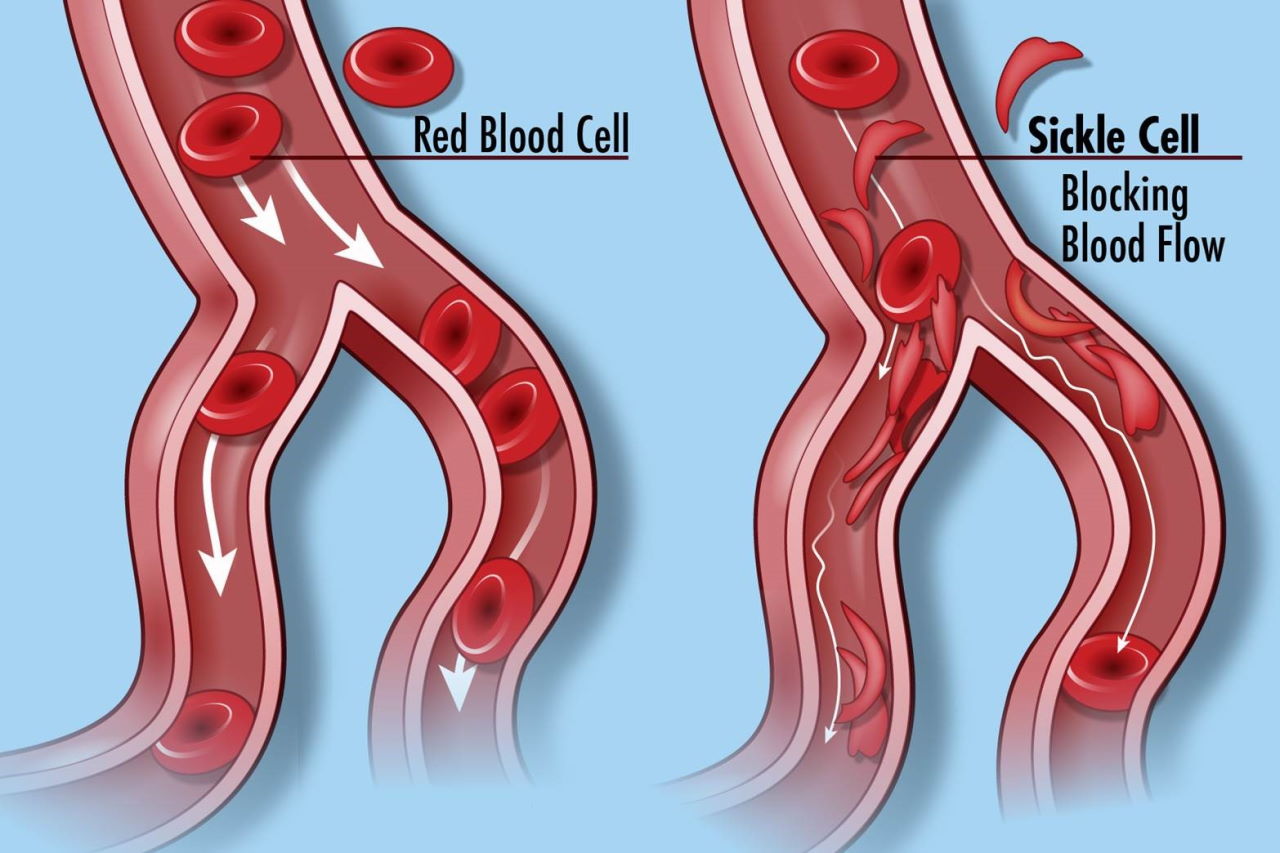
Нормальні клітини крові (ліворуч) і клітини крові при серповидноклітинній анемії. National Human Genome Research Institute / Flickr
Що лікують терапії?
Лікування серповидноклітинної анемії раніше було лише профілактичним, щоб запобігати важким ускладненням, у тому числі сильного болю та пошкодження органів, що називають вазооклюзійними кризами. Повторення цих криз може призвести до інвалідності та передчасної смерті. Це відбувається тому, що людина успадковує мутацію гемоглобіну — білка, що міститься в червоних кров'яних тільцях і транспортує організмом кисень. Еритроцити набувають форми півмісяця або ж серпа, чим обмежують потік у кровоносних судинах та перешкоджають нормальному постачанню кисню у тканини організму. Нові терапії, Casgevy та Lyfgenia, які схвалило FDA, допомагають хворим виробляти робочий варіант гемоглобіну.
Наскільки ефективними є лікування?
Casgevy та Lyfgenia виготовляються з власних стовбурових клітин крові пацієнта, які проходять генетичну модифікацію, а потім повертаються у вигляді одноразового внутрішньовенного введення. Різниця між препаратами полягає в способах модифікації та доставки редагованих стовбурових клітин. Casgevy є першою схваленою FDA терапією з використанням технології редагування геному CRISPR/Cas9. Генна терапія Lyfgenia, використовує як носій доставки генів лентивірусний вектор, який попередньо модифікують таким чином, щоб вірус не міг інфікувати клітини-господаря.
Результатом клінічних випробувань Casgevy за участю дорослих і підлітків з важкими повторюваними вазооклюзійними кризами, була відсутність цих больових епізодів щонайменше протягом 12 місяців під час 24-місячного періоду спостереження. Загалом цього результату досягли 93,5 відсотка пацієнтів. Найпоширенішими побічними ефектами були низький рівень тромбоцитів і лейкоцитів, нудота, м'язово-скелетний біль, біль у животі, головний біль, виразки в ротовій порожнині і свербіж.
Lyfgenia також оцінювали протягом 24 місяців на пацієнтах віком від 12 до 50 років. В результаті, 88 відсотків пацієнтів були позбавлені вазооклюзійних криз протягом 6 та 18 місяців після введення терапії. Побічні ефекти включали стоматит, низький рівень лейкоцитів, еритроцитів і тромбоцитів, що притаманно періоду після хіміотерапії. Втім, у пацієнтів також виникали злоякісні гематологічні захворювання (рак крові), тому пацієнтів попереджають про ризик інформацією на етикетці препарату.
- Першою генну терапію серповидноклітинної анемії на основі CRISPR ухвалила Велика Британія.