Минулого року медики мали значні успіхи в генній і клітинній терапії, які були наслідками багаторічної роботи науковців з усього світу. І тепер уже ці успіхи стануть підґрунтям для розвитку науки у 2026 році. На нього заплановані випробування вакцини від туберкульозу для дорослих, нових ліків від ВІЛ з довготривалим ефектом і терапій від агресивних видів раку. Редакція журналу Nature зібрала 11 клінічних випробувань, які формуватимуть науку у 2026 році, а ми розповідаємо, чому за ними варто стежити.
Довготривалий контроль ВІЛ
Хоча сучасні антиретровірусні препарати допомагають зупинити поширення вірусу імунодефіциту людини в організмі пацієнтів, вони потребують щоденного приймання протягом усього життя. Це тому, що вони не можуть приборкати вірус, який вже заразив імунні клітини та разом із ними потрапив у віддалені куточки організму.
Тому дослідники створили новий препарат на основі антитіл, який допомагає імунній системі розпізнавати інфіковані ВІЛ клітини та знищувати їх. Цей препарат випробовували за участі людей, у яких ВІЛ-інфекція виникла нещодавно, тож їхня імунна система ще не втратила здатність самостійно боротися із хворобами.
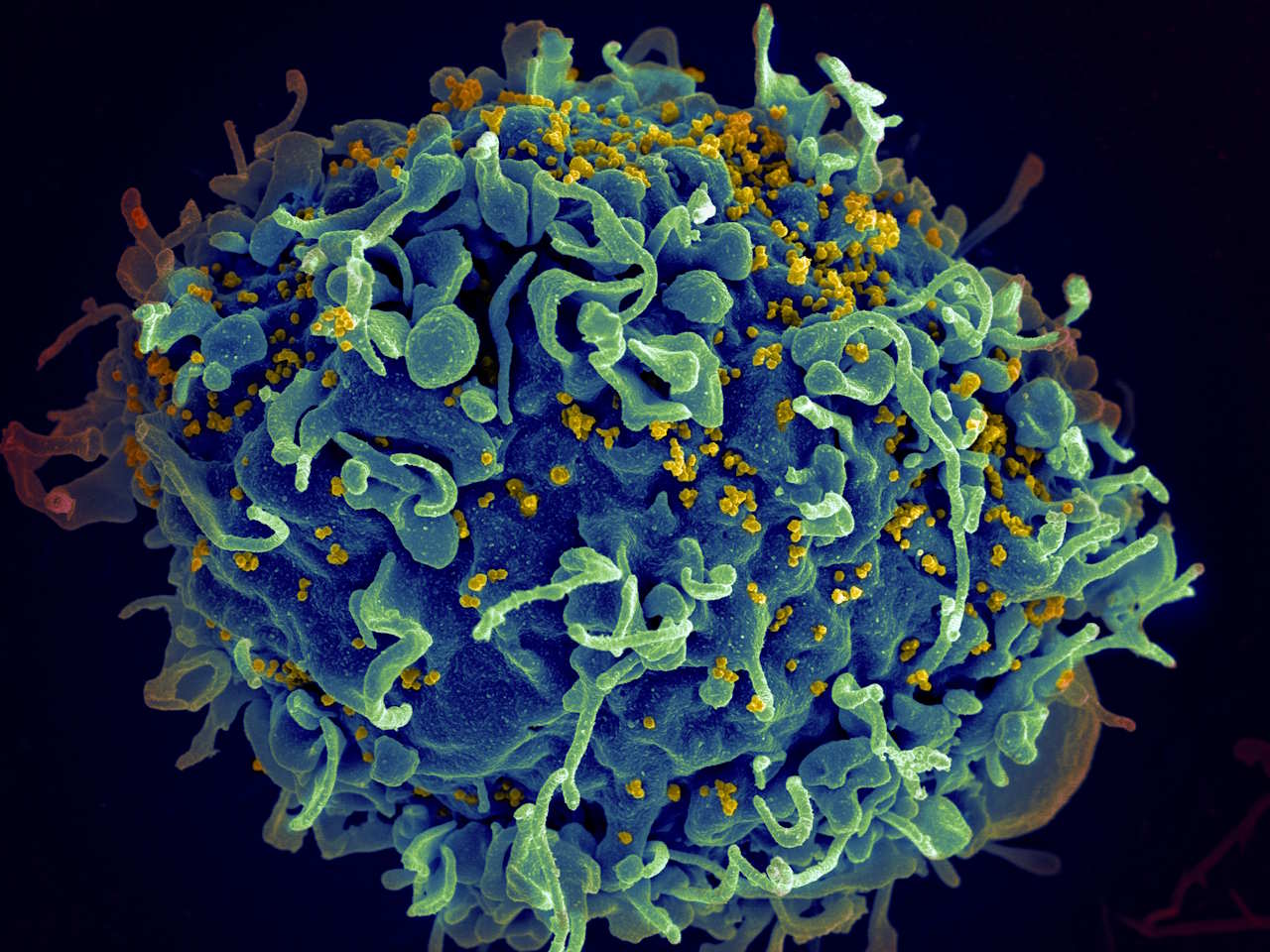
Інфікований ВІЛ Т-лімфоцит, на який не діють антиретровірусні препарати. Seth Pincus, Elizabeth Fischer, and Austin Athman / National Institute of Allergy and Infectious Diseases / National Institutes of Health
Ранні результати другої фази випробувань цього препарату представили минулого року: 75 відсотків пацієнтів, які отримали таке лікування, не мали частинок вірусу в крові протягом п’яти місяців, а деякі не потребували антиретровірусних ліків протягом двох років. У групі плацебо лише 11 відсотків людей позбулися вірусу на п’ять місяців. Надалі компанія-виробник препарату планує дослідити, чи поєднання з вакцинами й іншими терапіями ВІЛ позбавить пацієнтів потреби у щоденному прийманні антиретровірусних препаратів.
Дорогі ліки для рідкісної хвороби
У 2025 році науковці повідомили й про інший прорив у лікуванні імунодефіцитів, на цей раз вроджених. Компанія Prime Medicine за допомогою технології первинного редагування ДНК позбавила двох пацієнтів хронічної гранулематозної хвороби. Через рідкісну мутацію імунні клітини цих людей були нездатними до фагоцитозу — процесу, який допомагає позбутися бактерій і грибів, що спричиняють хвороби.
Зазвичай людям із таким діагнозом доводиться протягом усього життя приймати антибіотики та протигрибкові препарати профілактично. Але компанія змогла виправити мутацію в імунних клітинах, які спершу видалили з тіла цих пацієнтів, а потім повернули назад. Цього виявилося достатньо для відновлення роботи імунних клітин і зменшення запальних процесів в організмі пацієнтів.
Однак хронічна гранулематозна хвороба є рідкісною — наприклад, у США її мають лише тисяча людей, із яких лише 250 випадків спричинені саме тією мутацією, яку виправили за допомогою первинного редагування ДНК. Тому компанія Prime Medicine веде переговори з Управлінням з продовольства та медикаментів США, щоб зробити терапію більш доступною, а також, можливо, адаптувати її до інших рідкісних спадкових хвороб.
Коли організм сам собі ворог
Хвороби виникають не лише тоді, коли імунітет працює недостатньо добре, але й тоді, коли він надміру активний. Зазвичай такі автоімунні розлади лікують за допомогою препаратів, що пригнічують імунітет, але тоді виникає ризик інфекцій та інших ускладнень. Натомість компанія Cartesian Therapeutics почала випробовувати CAR T клітинну терапію, у якій одні імунні клітини націлюють на інші, що спричиняють хворобу.
Цей підхід застосували для лікування міастенії гравіс — захворювання, за якого організм пошкоджує зв’язки між нейронами та м’язами, через що хворі мають постійну втому та слабкість. У другій фазі випробувань майже 60 відсотків пацієнтів досягли ремісії за шість місяців, а більшість залишалися в такому стані й за рік після початку лікування.
Надалі компанія планує розширити кількість учасників клінічного випробування терапії, а також спробувати зробити її доступнішою. Таким чином клітинна терапія, спрямована безпосередньо на причину хвороби, може стати першою лінією лікування міастенії, а в майбутньому — й інших автоімунних захворювань.
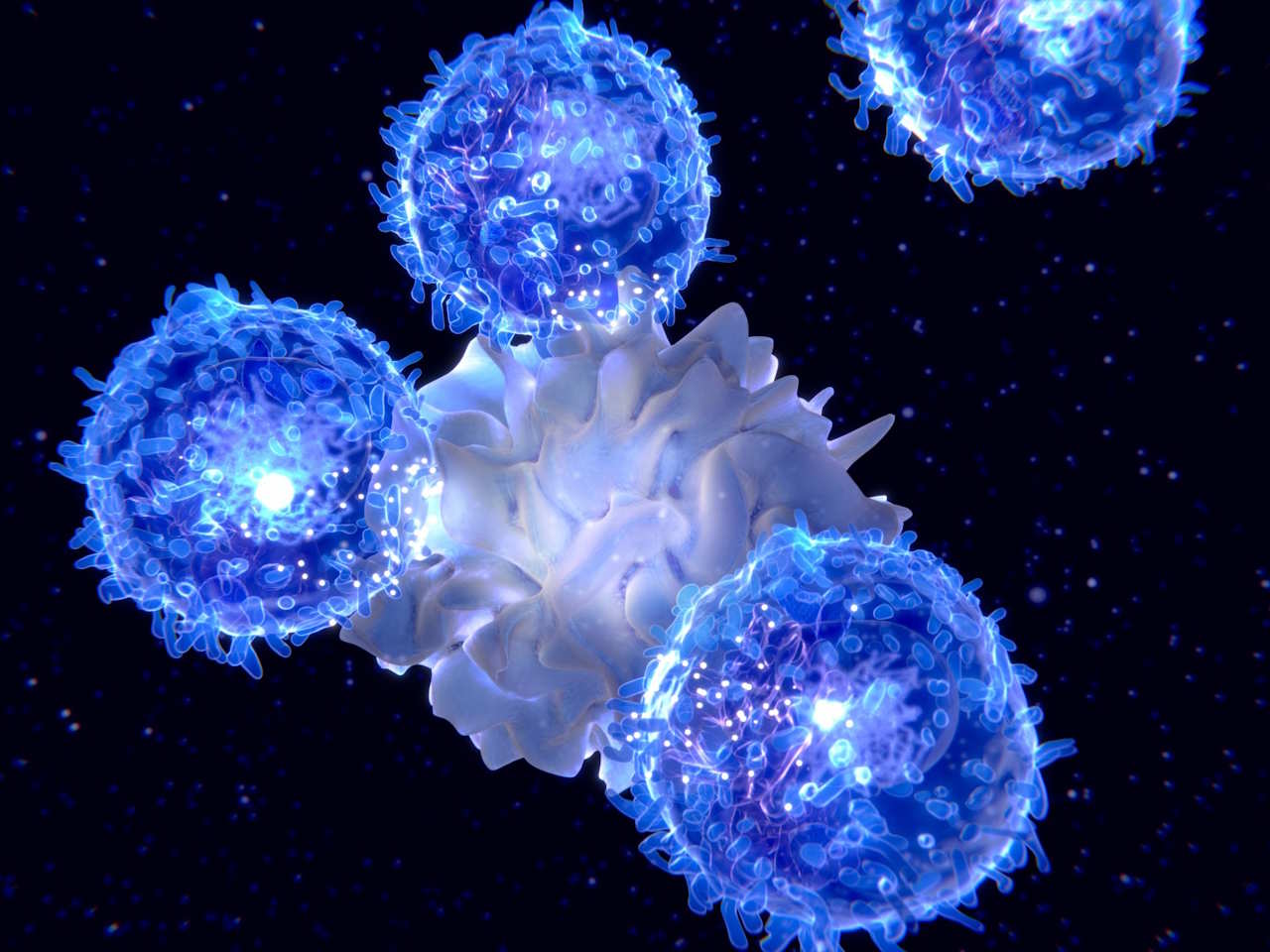
Дендритна клітина (в центрі) вказує Т-лімфоцитам на патогени. Міастенія гравіс, як і багато інших автоімунних захворювань, виникає через порушення таких взаємодій між різними імунними клітинами, внаслідок чого вони починають руйнувати клітини власного організму. Shutterstock
(Не)забуті тропічні хвороби
У 2026 році стануть відомими результати першого клінічного випробування вакцини від гарячки Ласса на людях.
Це геморагічна лихоманка, що за тяжкістю не поступається хворобам, спричиненим вірусами Ебола та Марбург. Щороку медики фіксують до 300 тисяч випадків зараження й до п’яти тисяч смертей, здебільшого на заході Африки, де гарячка Ласса є ендемічною та може передаватися через контакт із зараженими чи екскрементами гризунів.
Вакцину LASSARAB розробили у Центрі вакцин і підготовки до пандемій Джефферсона у США, адже збудник гарячки Ласса є й потенційним агентом біологічної зброї — зараз немає ані вакцин, ані ліків від цієї хвороби. Разом із гарячкою Ласса нова вакцина має захищати людей і від сказу, який також є серйозною загрозою для громадського здоров’я на заході Африки.
У першої тисячі учасників клінічного дослідження не виявили серйозних побічних ефектів від щеплення двома дозами, а також у них зросли рівні антитіл до вірусу. Дані про ефективність вакцини для запобігання хворобі збиратимуть ще до травня цього року, після чого доступ до неї в межах клінічних випробувань зможуть отримати більше людей.

Для створення вакцини усі роботи з вірусом Ласса, як і з іншими потенційними агентами біологічної зброї, проводять у спеціальних стерильних боксах. dpa picture alliance / Alamy
Одні ліки проти різних видів раку підшлункової
Хоча науковці вже протягом десятиліть знають, що більшість випадків раку підшлункової спричинені мутацією в гені KRAS, досі бракувало ліків, що могли б ефективно впливати на цю мутацію. А ті, що вже вдалося розробити, були націлені на рідкісну мутацію. Натомість цьогоріч мають стати відомими результати тестування нових ліків, які діють одразу на три різні мутації в цьому гені, охоплюючи можливості лікування для майже всіх пацієнтів із раком підшлункової.
Новий препарат від раку підшлункової, званий дараксонрасибом, знешкоджує мутований ген, зв’язуючи його з білком. У попередніх стадіях клінічних випробувань цей препарат спричинив лише помірні побічні ефекти — нудоту, діарею та запалення слизової рота. Це значно менше за перелік побічних ефектів традиційної хімієтерапії раку підшлункової, яка потребує багатьох препаратів і часто є недостатньо ефективною. Крім цього, препарат достатньо приймати у вигляді таблеток щодня, що робить його доступнішим за внутрішньовенні препарати для хімієтерапії.
Щоб рак молочних залоз не повертався
У 2026 році у 40 центрах по всьому світу продовжиться набір учасниць клінічного випробування клітинної імунотерапії раку молочних залоз із метастазами. У поєднанні з інгібіторами контрольних точок, що підсилюють імунну відповідь, клітинна терапія Bria-IMT покликана збільшити очікувану тривалість життя та час до рецидиву в жінок із метастазами раку.
У випробуваннях цієї терапії братимуть участь пацієнтки з різними типами раку та метастазами в різних частинах тіла, зокрема в мозку, які є одними з найважчих для лікування, а також ті, кому не допомогли попередні курси хіміє- чи імунотерапії. Це дозволить науковцям дізнатися, для яких жінок такий підхід є найбільш ефективним і порівняти його з уже стандартними методами лікування раку молочних залоз.
Вакцина від туберкульозу для дорослих
Хоча вакцина від туберкульозу, знана також як БЦЖ, входить до календаря обов’язкових щеплень, вона є ефективною лише в ранньому дитинстві. Водночас імовірність зараження туберкульозом збільшується саме в підлітковому та дорослому віці. І навіть попри розроблені методи лікування, щороку туберкульоз відбирає близько мільйона життів.
Тому дослідники створили нову довготривалу вакцину від туберкульозу, засновану на білку з поверхні клітин мікобактерії, що й спричиняє хворобу. У попередніх етапах клінічного випробування ця вакцина майже на половину зменшила темпи розвитку легеневої форми туберкульозу в людей, які вже були носіями бактерії.
У новому етапі дослідження, який проведуть у 2026 році, вакцину випробують за участі близько 20 тисяч людей у Південноафриканській Республіці, Кенії, Малаві, Замбії й Індонезії. Більшість з учасників вже є носіями інфекції, однак ефективність вакцини також оцінюватимуть у тих, хто ніколи не мав туберкульозу, і людей із ВІЛ-інфекцією.
Новий удар по «поганому» холестерину
Малорухливий спосіб життя та більш калорійна їжа призвели до того, що наразі серцево-судинні захворювання є головною причиною смертності в Україні та світі. Вагомим фактором цих хвороб є атеросклероз — стан, коли холестерин накопичується в стінках судин, зменшуючи їхню прохідність і збільшуючи ламкість.
У 2026 році стануть відомими результати клінічного випробування препарату пелакарсену, який націлений на зниження рівня ліпопротеїну a у крові пацієнтів. Це саме та форма холестерину, високий рівень якої пов’язують із розвитком атеросклерозу, інфарктів та інсультів.
У випробуванні беруть участь близько 7000 людей з різних регіонів світу, у яких оцінюватимуть не лише рівень ліпопротеїну a, але й частоту різних серцево-судинних захворювань. Крім цього, науковці порівнюватимуть, які переваги від приймання препарату матимуть люди з різним початковим рівнем холестерину — тобто, чи буде пелакарсен найбільш корисним для тих, хто вже має високий рівень холестерину та ризик хвороб серця.
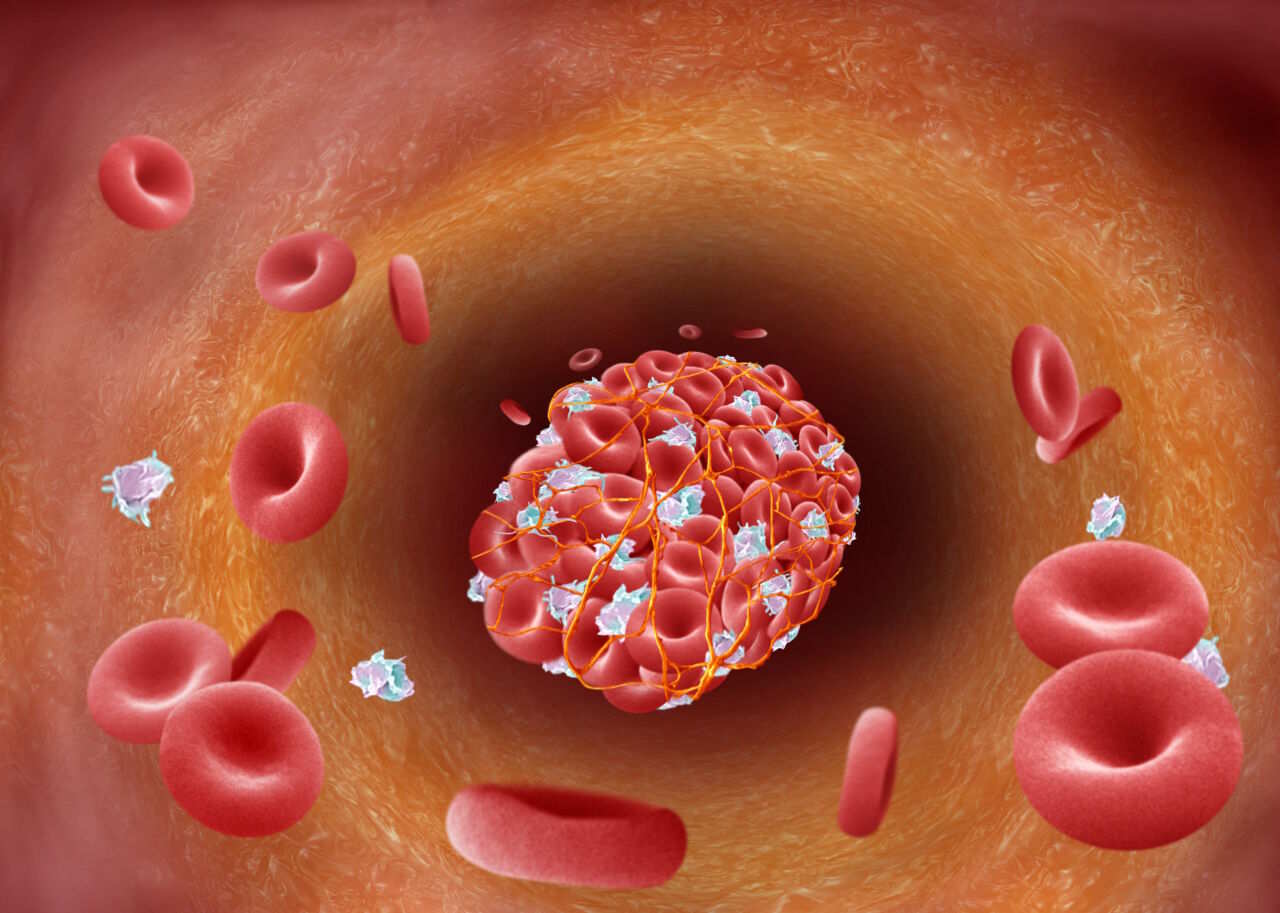
Атеросклероз звужує судини, внаслідок чого в них можуть утворюватися тромби, які призводять до інфарктів та інсультів. Annie Cavanagh / Wellcome Collection.
Не холестерином єдиним
Однак останніми роками науковці знаходили все більше підтверджень тому, що причиною атеросклерозу є не просто високий рівень холестерину, а ще й запалення в стінках судин. Саме його підозрюють у спричиненні розривів атеросклеротичних бляшок, які призводять до інфарктів та інсультів. Тому науковці націлилися на інтерлейкін-1 — сигнальну сполуку, що провокує запалення. Її блокування виявилося ефективним способом запобігання інфарктам та інсультам.
Але дослідники також помітили, що найвищий ефект від блокування інтерлейкіну-1 був у людей, які мали нижчі рівні інтерлейкіну-6, ще однієї прозапальної сполуки. Тому у 2026 році одразу три клінічні випробування, названі на честь грецьких богів, проводитимуть для препарату на основі антитіл, що блокує інтерлейкін-6.
Перше випробування, ZEUS, матиме на меті оцінити частоту серцево-судинних хвороб у пацієнтів з атеросклерозом, які приймають цей препарат. Друге випробування, HERMES, оцінюватиме ефективність препарату для запобігання повторним хворобам серця в людей із серцевою недостатністю, які вже мають залишкові запальні процеси в організмі. Третє клінічне випробування, ARTEMIS, допоможе визначити, наскільки корисним є введення антитіл до інтерлейкіну-6 пацієнтам, які пережили гострий інфаркт, безпосередньо після потрапляння до лікарні.
Стовбурові клітини для здоров’я мозку
Стовбурові клітини розглядають як один із методів лікування тих хвороб, для яких не існує інших, специфічних терапій. Такими є різні нейрологічні порушення, зокрема хвороби Паркінсона та Альцгеймера, бічний аміотрофічний і хронічний розсіяний склерози, інсульти та травми мозку, які заподіюють непоправну шкоду нервовим клітинам.
Уже у 2010-х роках лікарі помітили, що використання стовбурових клітин для відновлення пошкоджених очних нервів може полегшити прояви й інших, нейрологічних хвороб. Так з’явилася ідея NEST — клітинної терапії, за якої стовбурові клітини з кісткового мозку пацієнта вводять йому внутрішньовенно та в ніс, де знаходяться нерви, що ведуть до мозку.
Цей метод випробували вже на 200 пацієнтах, частина з яких відчула покращення здатності рухатися та говорити, а дехто навіть більше не потребував колісного крісла. А у 2026 році науковці продовжать збирати дані про те, наскільки тривалими є ці покращення.
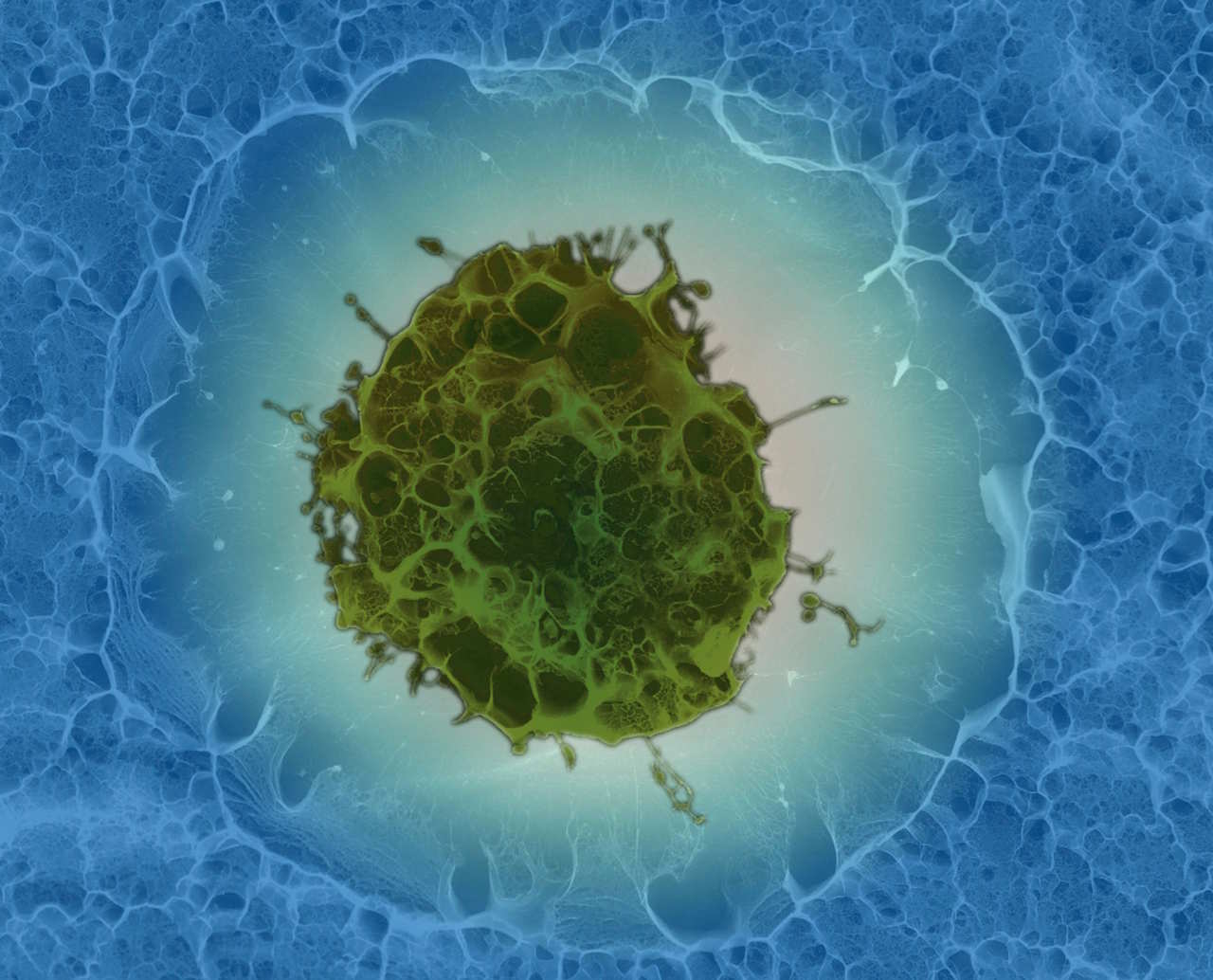
Сканувальна електронна мікроскопія стовбурової клітини — їх планують використовувати для відновлення рухових і розумових здібностей людей із нейрологічними порушеннями. Sílvia A Ferreira, Cristina Lopo and Eileen Gentleman, KCL / Wellcome Collection
Довга рука ковіду
У 2026 мине вже сім років від початку пандемії ковіду, але навіть після її завершення коронавірус не припинив бути загрозою для здоров’я людей у всьому світі. Частина пацієнтів зіткнулася з довготривалими наслідками інфекції, зокрема надмірною втомою, що супроводжувала навіть буденні заняття. Після коротких прогулянок у них уже виявляли зміни в показниках крові, які вказували на проблеми з дрібними судинами.
Британські медики почали випробовувати різні ліки, що могли б покращити стан хворих, які перенесли «довгий ковід». Серед них були протизапальні препарати та ті, що перешкоджають надмірному згортанню крові. Лікарі залучили молодих людей, які через хворобу на роки втратили здатність повноцінно займатися щоденними справами. Науковці планують оголосити результати цього випробування вже у 2026 році.