Європейські науковці представили вдосконалений електростимулятор спинного мозку, який дає змогу паралізованим людям відновити можливість ходити та виконувати інші звичні дії, як-от їздити на лежачому велосипеді або займатися веслуванням. Відмінністю нового стимулятора від схожих попередніх є його націленість на задні корінці спинного мозку, та керування ним за допомогою програмного забезпечення, що стимулює спинний мозок на активацію м'язів, потрібних для конкретної діяльності. Технологія показала свою дієздатність у випробуванні на трьох паралізованих пацієнтах, які завдяки їй змогли щонайменше самостійно пересуватися. Результати оприлюднені в журналі Nature Medicine.
Що таке електростимуляція спинного мозку і для чого застосовується?
Поки що пацієнти, які стикнулися з паралічем кінцівок через травму спинного мозку, мають мало доступних варіантів відновлення своєї рухової активності. Але зараз проходять випробування кілька технологій, які дають надію на повернення колишніх можливостей. Серед них — епідуральна електрична стимуляція. Вона полягає в імплантації до спинного мозку електродів, які здійснюють його електричну стимуляцію, та генератора електричних імпульсів під шкіру. Стимуляція у попереково-крижовому відділі вже показала свою ефективність у покращенні результатів фізичної реабілітації пацієнтів із паралічем нижніх кінцівок. Деякі з них навіть змогли завдяки цьому відновити здатність самостійно стояти та ходити. Але науковці з Лозаннського університету та Швейцарського федерального інституту технологій спільно з європейськими колегами захотіли, щоб електростимуляція спинного мозку могла повернути можливість ходити кожному такому пацієнтові.
Що зробили вчені для досягнення мети?
Науковці звернули увагу на те, що сучасні імплантати для стимуляції спинного мозку походять від технології, що початково розроблялася для полегшення болю. Зокрема, вони переважно сконструйовані таким чином, що націлюються більшою мірою на задні канатики спинного мозку, тоді як для відновлення рухової активності ефективнішою є стимуляція задніх корінців спинномозкових нервів. Обмежене охоплення задніх корінців знижує дієвість втручання, тому автори нової статті розробили новий, більш підхожих для цих цілей імплантат, який одразу може стимулювати 16 електродами 16 задніх корінців, які залучені до рухливості ніг та тулуба.
Щоб обрати оптимальне розташування електродів на спинному мозку, яке дозволило б отримати найкращі результати від стимуляції, науковці створили тривимірні моделі спинного мозку 27 дорослих людей на основі комп'ютерного та магнітно-резонансного сканувань. Аналізуючи індивідуальні відмінності в анатомії нервової системи, науковці виявили ділянки спинного мозку, розміщення електродів на яких має бути ефективним у більшості пацієнтів. Завдяки цьому вони створили оптимальний імплантат, утім, перед його встановленням все ще слід провести обстеження додаткове пацієнта, щоб визначити найбільш підхоже для кожного окремого випадку положення імплантату.
Наскільки нова технологія краща за попередні?
Перевірку вдосконаленої технології провели на трьох добровольцях, нижні кінцівки яких були паралізовані внаслідок аварії на мотоциклі. Спершу моделювання підтвердило, що найпоширеніший спинномозковий електростимулятор для знеболення, який є коротшим за новий на 19 міліметрів, не досягає усіх корінців пацієнтів, на які націлилися вчені для ефективної реабілітації. Тож далі науковці приступили до розроблення режиму електростимуляції, який теж є важливим чинником ефективності терапії. Результатом стало створення програмного забезпечення, яке визначає спосіб стимуляції спинного мозку (конфігурацію активних електродів), у залежності від типу виконуваної фізичної активності.
Зазвичай перші кроки паралізовані пацієнти здатні зробити після кількох місяців тренувань із електростимуляцією. Однак учасники цього дослідження вже у перші дні тестування змогли пройтися із додатковим підтриманням ваги їхнього тіла, зробивши до 300 кроків вже у перший день. Хоча більша частина рухів здійснювалася завдяки впливу електростимулятора, двоє учасників змогли частково контролювати свою ходу: коли їх попросили спробувати збільшити довжину кроку, їм вдалося керувати амплітудою рухів ногами.
Демонстрація рухових можливостей учасників з допомогою епідуральної електростимуляції. Andreas Rowald et al. / Nature Medicine, 2022
Позитивні результати надихнули вчених випробувати розроблену ними технологію і стосовно інших форм активностей. Тож вони розробили конфігурації стимуляції спинного мозку, які специфічні таким діям, як рухи ногами при плаванні, їзді на велосипеді, присіданні та жиму ногами тощо.
За п'ять місяців, що троє учасників випробовували технологію, вони суттєво вдосконалили свої навички та розширили репертуар можливих дій. Вони мали змогу керувати спинномозковим стимулятором самостійно, перемикаючи його за бажанням між режимами, наприклад, швидко перемкнутися зі стояння на ходьбу або навпаки. Якщо на початку пацієнтам обов'язково була потрібна допомога асистента для підтримання рівноваги та ваги тіла, то з часом вони пристосувалися до самостійної ходьби, опираючись на ходунки на колесах, та навіть могли кататися на лежачому велосипеді, який керується руками й ногами, та займатися веслуванням.
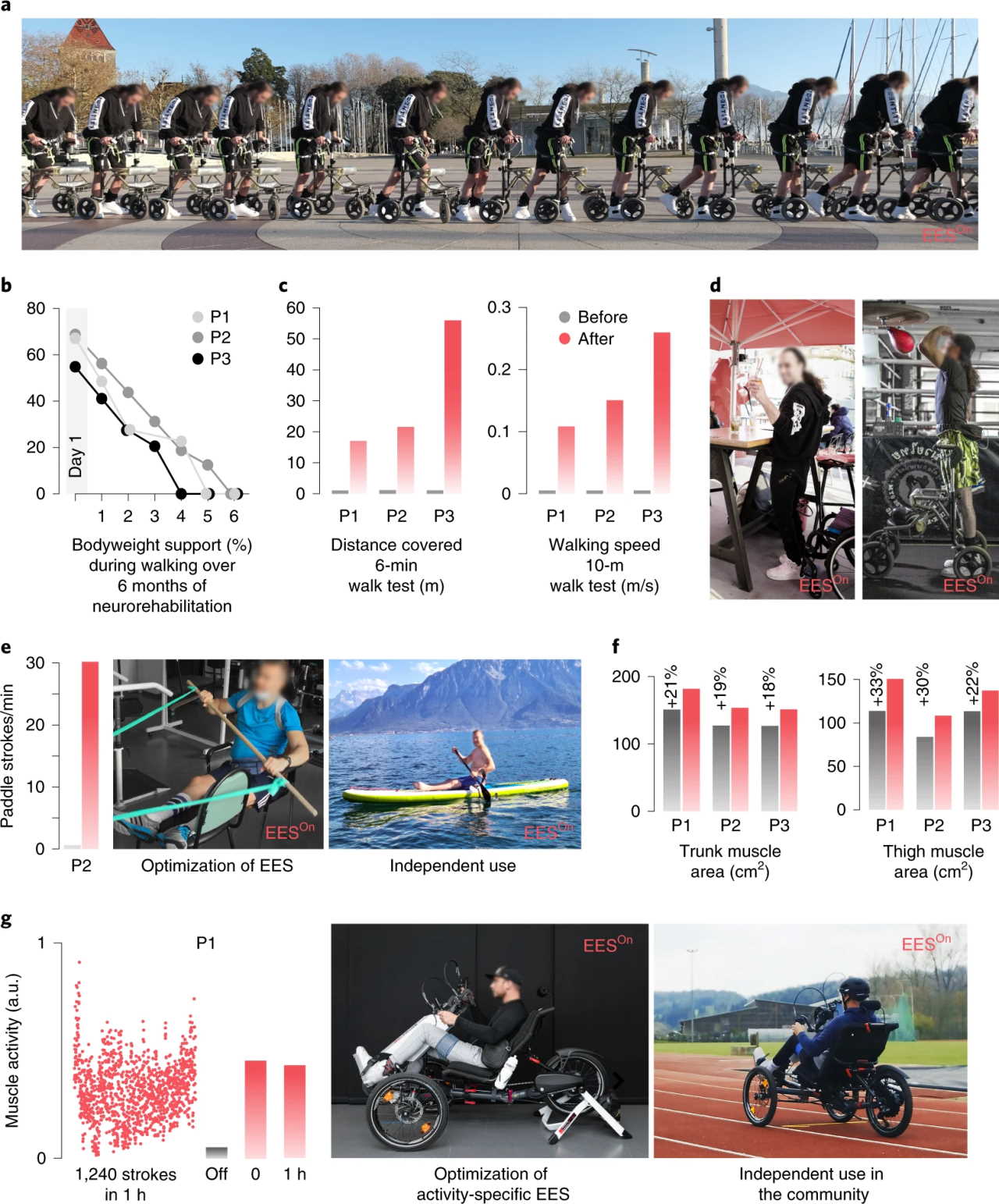
Відновлення звичайної активності пацієнтів з допомогою електростимуляції спинного мозку. Andreas Rowald et al. / Nature Medicine, 2022
Не менш важливо, що пацієнти відновили втрачену м'язову масу та посили її, причому не лише на ногах, а й на тулубі, що допомогло освоїти ще більше рухів та набути більшої самостійності. А двоє із учасників навіть частково повернули можливість контролю проксимальних м'язів ніг без електростимуляції. Вчені припускають, що у цих пацієнтів збереглася невелика кількість нервових волокон після травми, які під час малорухливого періоду життя залишалися нефункціональними, поки електростимуляція їх не активувала. Тож у майбутньому, із наступними вдосконаленнями технології, може стати реальністю відновлення повноцінного активного життя після серйозних травм спинного мозку за допомогою електростимуляції.