Американські науковці виявили відновлення спонтанного скорочення серцевих тканин після того, як вони були заморожені до трьох днів, а потім зігріті. Добитися цього вдалося завдяки застосуванню технології ізохорного суперохолодження, що дає змогу уникнути формування руйнівних кристалів льоду в заморожених клітинах. Результати, які можуть посприяти довшому збереженню донорських органів, опубліковані в журналі Communications Biology.
Навіщо нам технології замороження органів?
Хоча трансплантологія є однією з активно досліджуваних наук, протягом тривалого часу вона упирається об обмежений час придатності донорських органів після їх вилучення з тіла. Навіть у США із розвиненою системою охорони здоров'я, понад 70 відсотків органів для трансплантації утилізуються через неможливість їх зберегти протягом достатнього часу до проведення операції. Наприклад, донорські серця у середньому зберігають життєздатність усього 4-6 годин з моменту вилучення, за умови їх охолодження льодом.
Потенційно допомогти може глибоке замороження, яке здатне зберегти тканини протягом років. Але якщо наразі навіть є методи такого заморожування, то проблема із розмороженням поки що не розв'язана. При охолодженні тканин до температури, нижчої за нуль градусів за Цельсієм, в них починають формуватися кристалики льоду, які пошкоджують клітини. Тому при розмороженні вони можуть виявитися непридатними для пересадження. Нову технологію, яка дає змогу обійти це обмеження, представили вчені з Каліфорнійського університету в Берклі.
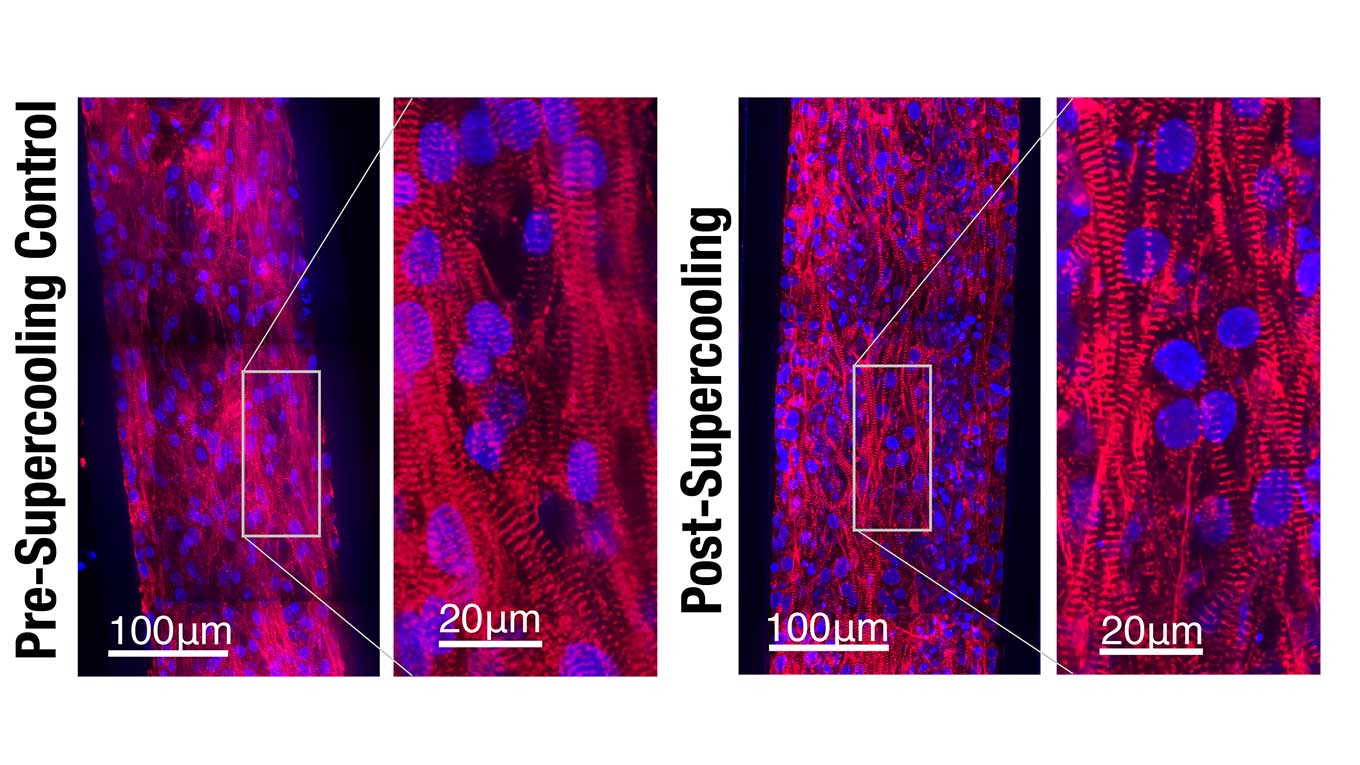
Отримані за допомогою конфокального мікроскопа зображення серцевих саркомерів до (зліва) та після (справа) охолодження. Matt Powell-Palm / UC Berkeley
Яка технологія краще зберігає органи свіжими?
Щоб уникнути утворення руйнівних кристаликів льоду, вчені застосували метод ізохорного суперохолодження. Воно характеризується термодинамічним процесом, за якого спостерігається сталий об'єм усередині ізохорної камери. У таких умовах кристалам льоду просто не вистачає місця для формування, навіть за температури, значно нижчої за нуль. Щоб це здійснити, зразок необхідно помістити в щільний контейнер з ізотонічним розчином, а потім герметично його закрити та позбавити повітря.
Сподіваючися у майбутньому подовжити життєздатність донорських сердець, вчені перевірили технологію на серці на чіпі. Це система серцевих тканин, вирощених у лабораторії з людських стовбурових клітин. Її особливістю є наявність притаманного справжньому серцю спонтанного скорочення та забезпечення тканин поживними речовинами через мікроканали, що імітують роботу кровоносних судин. У процесі дослідів науковці охолодили зразки серця на чіпі в ізохорній камері до мінус трьох градусів за Цельсієм. Відтак тканини відбирали через 24, 48 або 72 години й зігрівали за температури 37 градусів Цельсія для вивчення функціональності.
Що стало з тканинами серця після замороження?
У середньому 50-65 відсотків тканин добре пережили замороження й відновили спонтанне скорочення після зігрівання. Найбільша частка таких сердець на чипі була серед тих, що охолоджувалися на 24 години (65 відсотків), а найменше — серед заморожених на 48 годин (50 відсотків). Так само, близько 50-70 відсотків тканин продемонстрували нормальну реакцію на зовнішнє електричне подразнення та медичні препарати, незалежно від тривалості охолодження. Додатково 5-15 відсотків сердець на чіпі показали часткове відновлення функції скорочення, а в решти 20-40 відсотків її не помітили зовсім. Вчені відмітили, що охолодження не спричинило структурних змін у тканинах, але дещо подовжило тривалість скорочення, наслідки якого наразі залишилися нез'ясованими.
Вчені вважають, що їхня робота демонструє потенціал ізохорного суперохолодження для зберігання донорських органів. Вони наголошують на необхідності подальших досліджень на більших тканинах та органах, щоб перевірити їхнє припущення.