Канадські вчені змінили групу крові донорських легень із другої на першу, яка вважається універсальною, обробивши органи ферментами. Це дало змогу обійти бар’єр імунонесумісних трансплантацій за системою груп крові ABO. Під час моделювання трансплантації таких легень поза організмом вдалося запобігти розвитку запалення, що потенційно може зменшити ризики відторгнення трансплантату. Результати дослідження опубліковано в Science Translational Medicine.
Чому це важливо?
Для пацієнтів із термінальними стадіями легеневих захворювань успішна трансплантація легень є чи не єдиним способом лікування. Водночас можливість проведення трансплантації залежить від використання донорських органів, антигени на поверхні клітин яких мають бути імунологічно сумісними з організмом реципієнта. У протилежному випадку відбувається відторгнення трансплантата імунною системою реципієнта. Така умова імунної відповідності часто зменшує ймовірність знайти сумісного донора, що призводить не лише до збільшення смертності пацієнтів у списках очікування, але й до вибракування несумісних донорських органів.
Важливим фактором, що впливає на придатність легень для трансплантації пацієнту є сумісність групи крові донора та реципієнта. За системою ABO вона визначається A, B, та H антигенами, що знаходяться на поверхні еритроцитів. Так, перша група крові містить лише неімуногенний антиген Н, тому її часто називають універсальною групою крові, яку можна переливати людям з іншими групами. Друга та третя групи містять антиген А або В відповідно, а до складу четвертої групи крові входять одночасно антигени А і В, через що їх не переливають людям із першою групою крові. Тому кандидати на трансплантацію легень із першою групою крові в середньому чекають на донора довше й мають на 20 відсотків вищий рівень смертності, ніж особи з іншими групами. Задля зменшення ризику імунної несумісності трансплантата з організмом реципієнта група канадських вчених спробувала перетворити антиген A на поверхні клітин легень донора в універсальний антиген H за допомогою нещодавно ідентифікованих специфічних ферментів — деацетилази FpGalNAc і Fp-галактозамінідази.
Як створити «універсальні» легені для трансплантації?
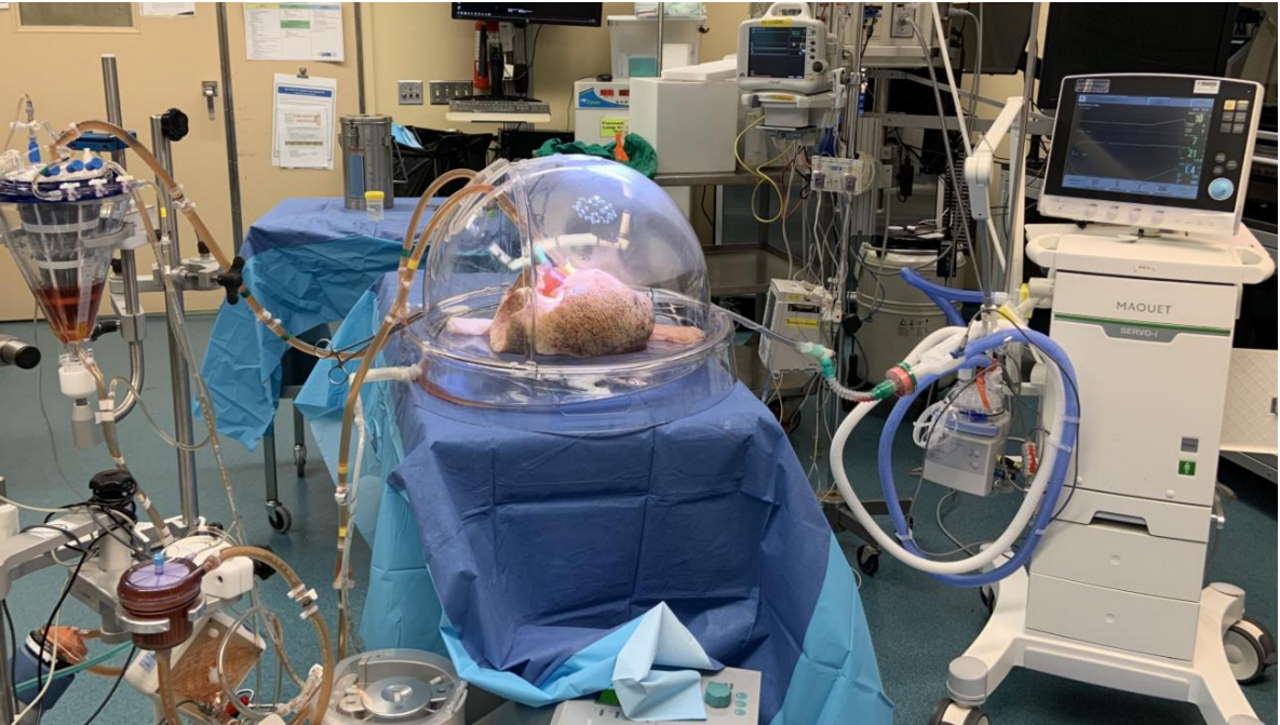
Створення «універсальних» легень проходило у два етапи. Спочатку вченим довелося тестувати ферментативне відщеплення антигену А на п’яти зразках еритроцитів, тканинах трьох аорт, а також на вісьмох легенях, отриманих від донорів із другою групою крові. Дослідження легень проводили за допомогою стандартного в трансплантології методу перфузії — підтримання органів живими поза організмом у спеціальній камері з розчином (EVLP).
На другому етапі дослідження вчені імітували трансплантацію легень поза організмом, де замість реципієнта з першою групою крові використали сурогатний розчин з доданою до нього плазмою першої групи крові. Для цього спочатку кожну з трьох пар донорських легень розділили на експериментальну та контрольну групи. В експериментальній групі легені обробляли ферментами, щоб перетворити антиген А на неімуногенний Н, а в контрольній — легені залишили необробленою. Для імітації трансплантації до розчину, у якому знаходилися легені обох груп, додали плазму першої групи крові. Контроль ферментативної реакції здійснювали на клітинному, тканинному та органному рівнях. Стан легень оцінювали за фізіологічними параметрами, а також проводили біопсію. Запальний процес визначали за гострим ураженням легень та зміною профілю компонентів імунної відповіді (системи комплементу, цитокінів, інтерферону).
Які результати дослідження?
На клітинному рівні після 30 хвилин інкубації еритроцитів із ферментами за фізіологічних умов було видаленню більш ніж 95 відсотків антигену А. У ході дослідження концентрація деацетилази FpGalNAc і Fp-галактозамінідази становила 1 мікрограм на мілілітр. Важливо було також продемонструвати ефективність видалення антигенів на тканинному рівні перед масштабуванням методу. З цією метою було використано тканини аорти людини, що їх інкубували з концентрацією ферментів на тому ж рівні, що й у попередньому досліді. Оброблення аорт за таких умов призвело до видалення 92 відсотків антигену А. На рівні утримуваних поза організмом людини легень показник ферментативного видалення антигену А становив більш ніж 97 відсотків. Водночас не було зафіксовано жодних змін маркерів запального процесу, що свідчило про нормальне функціонування легень після обробки ензимами.
Подальше моделювання трансплантації органів показало, що попередньо оброблені в такий спосіб легені характеризуються ефективним пригніченням ранніх фаз запалення та мінімізацією процесу відторгнення. За результатами біопсії вміст та концентрація циркулюючих факторів системи комплементу суттєво не відрізнялися між двома групами, однак у контрольній було виявлено порівняно вищі концентрації запальних цитокінів та інтерферону. Фізіологічні показники легень майже не відрізнялися в обох групах.
Попри те, що плазма крові дала змогу змоделювати потенційного реципієнта, у майбутньому застосування цільної крові та дослідження можливої реекспресії антигенів клітинами трансплантата дозволять точніше оцінити потенційне клінічне значення отриманих результатів щодо зменшення ризиків імунної несумісності.
Раніше ми вже писали про успішні випадки трансплантації людині серця, а також однієї та одразу двох нирок генетично модифікованої свині.