Трансплантація фекальної мікробіоти від молодих мишей до старих змінила показники запалення в мозку та сітківці, цілісності кишківника та метаболічний профіль, уподібнивши їх до таких у молодих мишей. Результати дослідження британських вчених підкріплюють думку про тісний зв'язок між кишківником та нервовою системою і можливість забезпечити здоровіше старіння втручанням до кишкового мікробіому. Статтю оприлюднили в журналі Microbiome.
Яким чином мікроби стосуються старіння?
Старіння — багатогранний процес, який зачіпає функціонування організму на різних рівнях. Воно відбивається на роботі органів, когнітивних здібностях та навіть мікробіомі. Склад та співвідношення мікробів у кишківнику підтверджено змінюється не лише в залежності від харчування, а й з плином років. Це нормальне явище, яке раніше вже пов'язували зі здоровим старінням, у ході якого відбувається набуття індивідуальних рис кишкового мікробіорізноманіття. Не у всіх цей процес відбувається як слід, але деякі дослідження вказують, що допомогти зі здоровим старінням або навіть його сповільненням може трансплантація фекальної мікробіоти. У дослідах на мишах з'ясувалося, що після перенесення старим мишам фекальних трансплантатів від молодих у них сповільнюється старіння мозку й стала краще працювати імунна система. Вчені Інституту Квадрам та їхні колеги теж перевірили, які наслідки на старіння матиме пересадка кишкового мікробіому.
Що й кому трансплантували?
Науковців цікавило, як трансплантація мікробів вплине на нервову систему, особливо мозок та очі, які сильно чутливі до стресових факторів, зокрема, до запалення, яке з віком наростає в організмі. Дослідження провели на лабораторних мишах трьох груп різних вікових категорій: молодих (3 місяці), старших (18 місяців) і старих (24 місяці). Частина тварин спочатку пройшли курс антибіотикотерапії, щоб вбити вже наявний кишковий мікробіом, а потім отримали оральний розчин фекальних трансплантатів від мишей іншої вікової категорії або однолітків або взагалі нічого не отримали, окрім антибіотика чи сольового розчину. Зміни в складі кишкової мікробіоти регулярно перевіряли протягом наступних 18 днів, секвенуючи ДНК у випорожненнях тварин. Стан кишківника, сітківки та мозку вивчали за допомогою аналізів крові, поведінкових тестів та імуногістологічних методів.
Що стало з мишами після процедур?
Типово, у старших та старих мишей сильніше проявляються маркери нейрозапалення в мозку, як-от активовані мікрогліальні клітини. Однак схожі показники знайшли у молодих мишей, що отримали мікробіоту від 24-місячних родичів, чим вони явно вирізнялися від інших однолітків. Натомість у старших і старих мишей, які отримали мікроби молодих, спостерігали помітне зниження маркерів нейрозапалення, у порівнянні з необробленими однолітками. Утім, це не допомогло їм краще проходити лабіринт на оцінювання пам'яті.
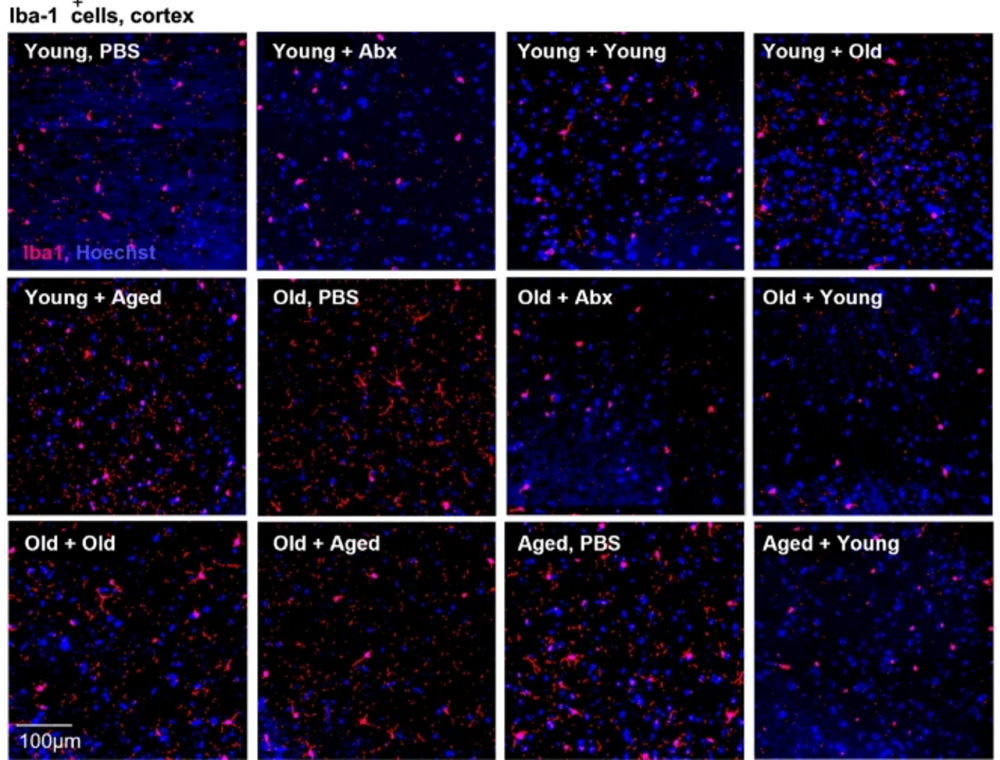
Кількість активованих клітин мікроглії (червоні) у корі молодих, старших та старих мишей, які отримали лише сольовий розчин (PBS), лише антибіотики (Abx) або фекальні транспланти від молодих, старших або старих мишей. Aimée Parker et al. / Microbiome, 2022
Зміни в стані сітківки теж відмітили. Якщо на початку дослідження у сітківці старих мишей був суттєво більший рівень запального білка С3, що пов'язаний із дегенерацією сітківки, ніж у молодих, то після перенесення їм мікробів молодих тварин він прирівнявся до такого у донорів. Протилежне відбулося у молодих мишей, що їм дали мікроби старих: рівень С3 у їхніх сітківках став подібним до такого у 24-місячних гризунів. Схожою була картина із іншими прозапальними молекулами сітківки. Натомість із білком RPE65, який критично важливий для нормального функціонування сітківки, але його рівні з віком зменшуються, все відбувалося навпаки: мікробіом молодих тварин допомагав збільшити його кількість, тоді як старих — зменшував.
Зрештою, трансплантація не могла не вплинути на структуру кишківника. У молодих мишей після перенесення їм мікробіому старих мишей спостерігалося збільшення, у порівнянні з необробленими контрольними однолітками, на 30 відсотків білка I-FABP, що є показником порушення цілісності епітелію кишківника та його підвищеної проникності. Тоді як у старих мишей після трансплантації фекалій 3-місячних мишей рівень I-FABP знизився на приблизно ті ж 30 відсотків, якщо порівнювати з іншими однолітками. Рівень білка LBP, який вивільняє печінка при просочуванні бактерій з кишківника, був вдвічі вищий у старих мишей і став приблизно таким же у молодих після отримання мікробів від старих тварин. Водночас у старих мишей LBP знизився до рівня молодих після трансплантації їхнього мікробіому. З іншими маркерами запалення в кишківнику ситуація була схожою.
За аналізами крові, трансплантація вплинула й на метаболічні шляхи. Молодий мікробіом призвів до збільшення кількості ліпідів та вітамінів у старих мишей, але старий — до зменшення показників у молодих.
Підсумовуючи, трансплантація калу від молодих мишей старим призвела до омолодження профілів запалення мозку та сітківки, а також цілісності кишківника та метаболізму. Результати підкріплюють думку, що прицільна зміна кишкової мікробіоти для модуляції імунних та метаболічних процесів може допомогти зменшити системне запалення та посприяти здоровішому старінню. Проте наразі сказати достеменно, чи так само відбувається і в організмі людей, неможливо. Чому не завжди можна екстраполювати результати досліджень на мишах на людей, ми писали в матеріалі «Про мишей і людей».