Американські вчені описали технологію керування активністю нейронів у мозку тварин за допомогою ультразвуку. Внесенням високочутливого до ультразвуку білка в мозок мишей вони змогли контролювати активність рухових нейронів тварин, неінвазивно впливаючи на їхній череп сфокусованим ультразвуком. Технологія може стати зручним аналогом оптогенетики та посприяти розробленню терапії проти низки захворювань у людей. Дослідження опублікували в журналі Nature Communications.
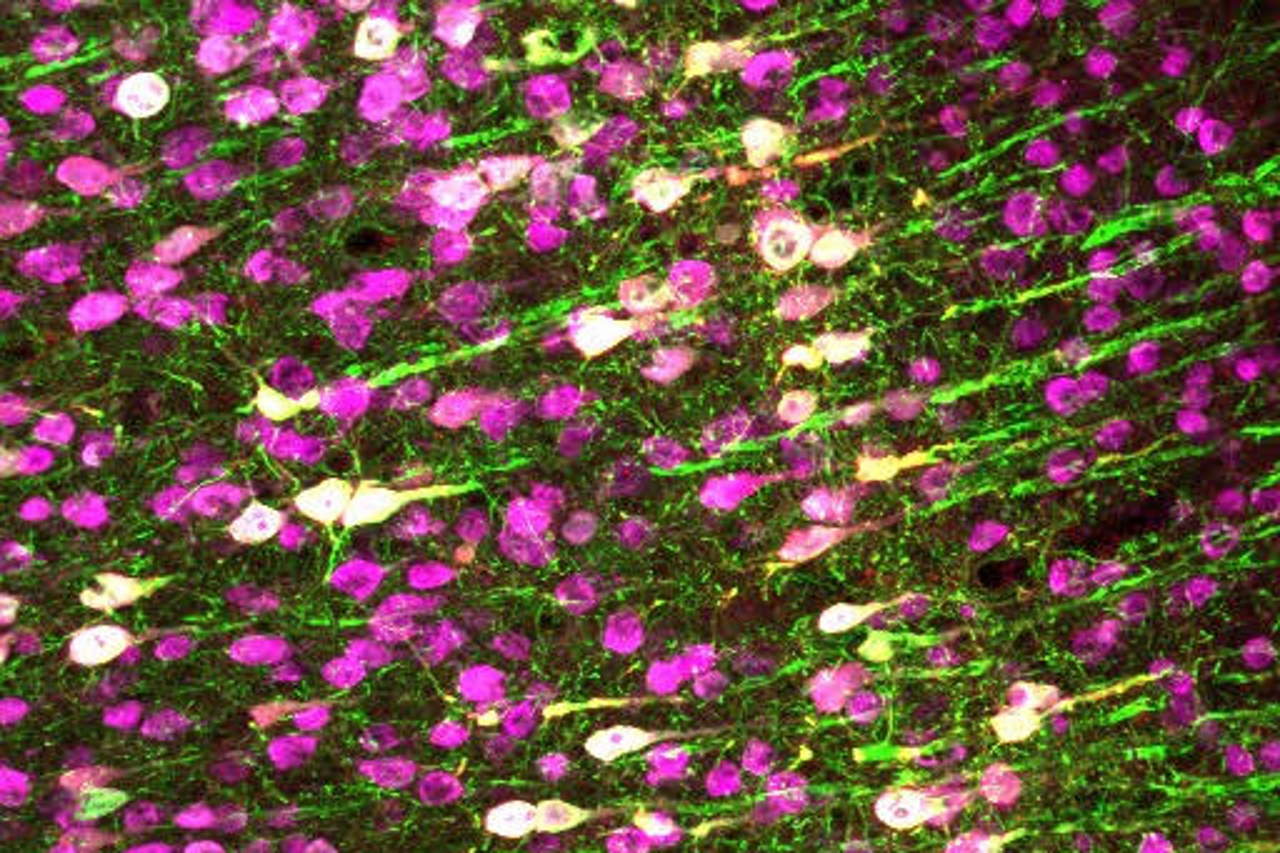
Експресія TRPA1 (білий) та зеленого флуоресцентного білка (зелений) нейронами мишей (рожеві). Salk Institute
Що таке оптогенетика й навіщо керувати нейронами?
Однією із технологій нейробіологів, яка зараз активно вивчається, зокрема як потенційний засіб для лікування низки нервових та психічних захворювань, є оптогенетика. Це спосіб керування активністю клітин світлом. Він полягає у внесенні в бажані нервові клітини генів світлочутливих білків, завдяки чому, впливаючи на них світлом із відповідними довжинами хвиль, можна активувати або пригнічувати їхню роботу. Тому оптогенетика допомагає вивчати роль окремих нейронів та їхніх мереж у нормальних та патологічних процесах нервової системи, а також могла б допомогти лікувати хвороби, які спричинені неправильною роботою клітин. Минулого року технологію навіть використали на людині, змінивши клітини сітківки чоловіка та частково повернувши йому втрачений зір. Але для підсвічування клітин мозку потрібно доставити те світло всередину черепної коробки, що зазвичай досягається імплантацією до неї оптоволоконних кабелів або окремих пристроїв зі світлодіодами, і зі зрозумілих причин, це ускладнює роботу. Однак вчені з Інституту біологічних досліджень Солка та Каліфорнійського університету в Сан-Дієго представили у новій роботі інший підхід, що дає змогу керувати клітинами мозку неінвазивно.
Що пропонують замість оптогенетики?
Ще у 2015 році науковці опублікували статтю, де описали можливість керувати нейронами нематод Caenorhabditis elegans за допомогою зовнішніх ультразвукових коливань частотою від 500 кілогерців до 2 мегагерців. Для цього в клітини тварин було внесено ген білка-механорецептора TRP-4. Підхід, названий соногенетикою, здавався обнадійливим, оскільки ультразвук вже тривалий час застосовується у медицині та біомедичних дослідженнях, зокрема для стимуляції кори мозку крізь непорушений череп. Крім цього, ультразвук можна легко сфокусувати, піддаючи впливу лише невеликий об'єм тканин, залишаючі навколишні тканини недоторканими.
Однак з'ясувалося, що в тканинах ссавців спосіб працює не ідеально — доводиться жертвувати або площею оброблення тканин, або глибиною, на яку здійснюється вплив, а значить і ефективністю самого впливу. Тому що хоч ультразвук випробуваної частоти, до якої чутливий білок, і здатний проникати на достатню глибину, але його важко сфокусувати на невеликі частини мозку. Щоб обійти це обмеження, науковці захотіли знайти інші білки, які забезпечать клітини ссавців чутливістю до ультразвуку вищої частоти. Наприклад, до оптимальних 7 мегагерців, які за попередніми дослідженнями, проникають крізь тканину мозку гризунів і водночас їх можна сфокусувати до 107 кубічних мікрометрів.
Аналізуючи базу даних природних білків, що можуть мати необхідну чутливість до ультразвуку, вчені натрапили на 191 потенційно підхожий білок. Перевіривши їхні властивості в культурі людських ембріональних ниркових клітин, вони дійшли висновку, що найбільш чутливим до ультразвуку заданої частоти є людський білок TRPA1. Клітини із експресією цього білка втричі активніше реагували на ультразвук, у порівнянні з клітинами з мишачим варіантом TRPA1.
Як використали людський білок?
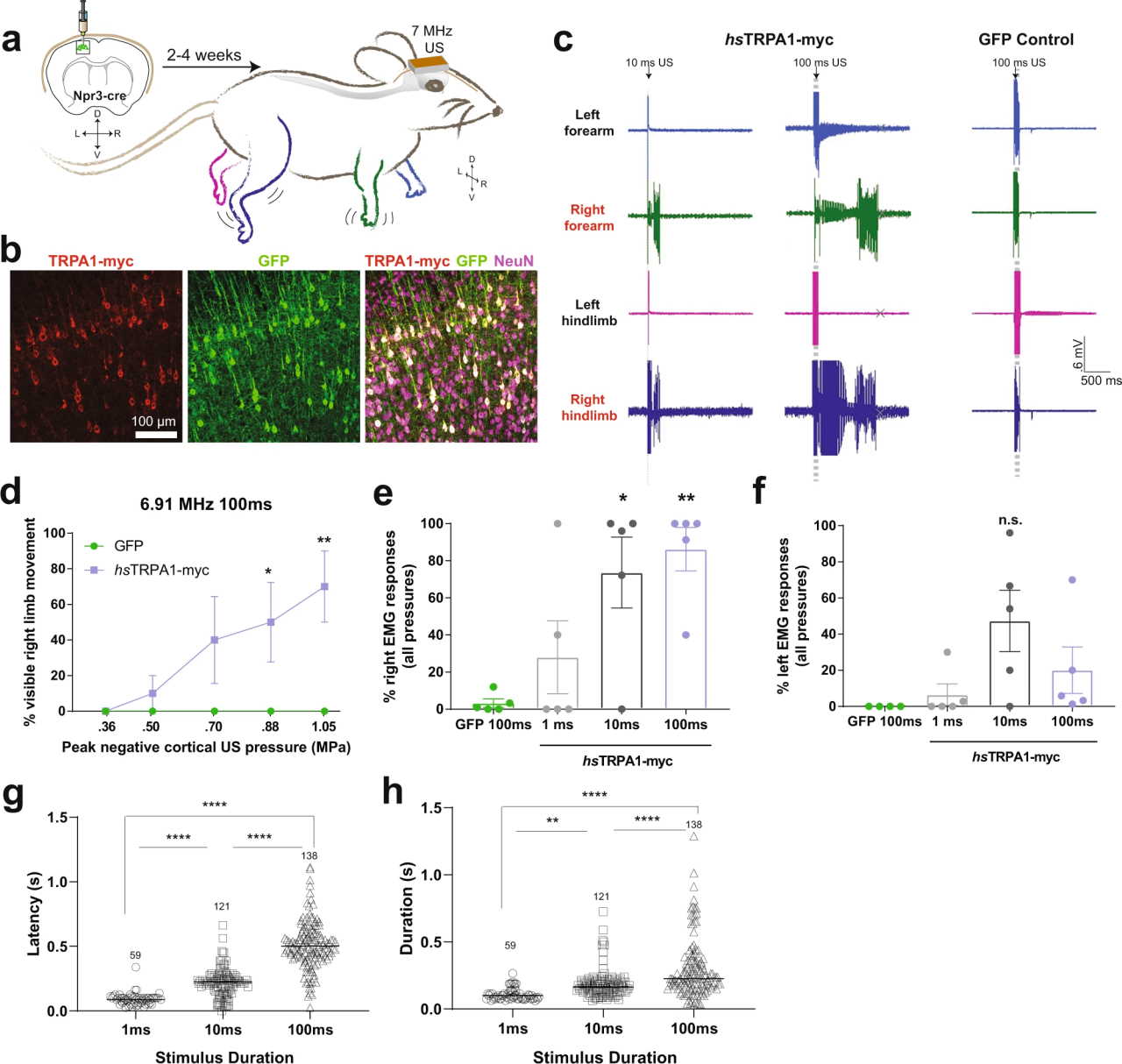
Надалі вчені перевірили, чи можна використати людський TRPA1 як інструмент соногенетики. Тож вони ввели ген білка п'ятьом мишам у рухові нейрони п'ятого шару кори головного мозку з допомогою внутрішньочерепної ін'єкції, а ще п'ятьом ввели лише ген зеленого флуоресцентного білка (GFP). Через декілька тижнів почали спостерігати, як змінюється активність нейронів та поведінка тварин у відповідь на вплив імпульсів ультразвуку з частотою 7 мегагерців тривалістю 1-100 мілісекунд, спрямованих на череп.
У тварин, у чиї нейрони ввели людський TRPA1, під впливом ультразвуку спостерігалися дозозалежні реакції м'язів, зокрема рухливість кінцівок. Тоді як у тварин, що отримали лише ген флуоресцентного білка, подібної реакції на ультразвук не відмітили. Отже, ультразвуком та білком TRPA1 можна керувати активністю нейронів у ссавців через непорушений череп. Причому технологія показала себе безпечною, оскільки модифіковані тварини з двох груп однаково проходили й навчалися в завданнях на рухливість, а годинна стимуляція ультразвуком згаданої частоти не пошкодила їхній гематоенцефалічний бар'єр.