«Яка іронія», — усміхається Тім Грінамайр. Багато років він проводив експерименти, спричиняючи у мишей стан, подібних до хвороби Паркінсона. Тепер хвороба прийшла до нього самого — людини, яка витратила половину життя на дослідження і пошук ліків проти неї. Як це — стати власним піддослідним, відчути на собі ту напасть, від якої намагався захистити інших? Що ми сьогодні знаємо про хворобу Паркінсона і як далеко ліки проти неї? Таку історію розповідає кореспондент журналу Science, яку ми для вас коротко переказали.
Діагноз
Кілька років тому нейронауковець і лікар Тім Грінамайр з Пітсбурзького університету став помічати тривожні симптоми у тілі. У нього пропав нюх. Він почав страждати від запорів. Він кричав і бився уві сні. Його ліва рука природно не розгойдувалася при ходьбі. Коли Тім звернувся до лікаря, той лише підтвердив діагноз, який він і так підозрював: у 67-річного чоловіка розвивалася хвороба Паркінсона.
Дізнавшись про свій діагноз, Тім сильно занепокоївся, як сприймуть цю новину близько 200 його пацієнтів із тією ж недугою. Більшість із них дізналося про це лише з виходом цієї статті. Лікар хвилювався, що його стан несправедливо перетягне на себе увагу пацієнтів.
У лікуванні своїх пацієнтів, Грінамайр покладався на досягнення медицини віком понад 50 років. Воно основане на використанні препарату з активною речовиною дофаміном. Саме з руйнуванням у чорній субстанції мозку нейронів, які виділяють цю речовину, пов'язують прояви хвороби Паркінсона — такі як тремор, порушення координації та мовлення, деменцію. Препарат не виліковує, а допомагає зменшити прояви, проте з часом і ця його дія згасає, і він має високий ризик важких побічних ефектів, серед яких неконтрольовані рухи.
Дослідження останніх десятиліть не раз давали надію, що невдовзі з'явиться нове лікування, здатне не просто замаскувати хворобу Паркінсона, а усунути її причину. Утім, для Грінамайра та його пацієнтів це відкриття може відбутися занадто пізно. На момент, коли хворобу вдається діагностувати, вона вже десятиліття як почала тихий розвиток на рівні клітинних механізмів. І все ж, Тім зазначає, що це найкращий час в історії для діагностування хвороби Паркінсона, зважаючи на всі досягнення науки до цього часу.
Початок шляху
Грінамайр почав свою кар'єру з дослідження механізмів розвитку хвороби Альцгеймера та хвороби Гантінгтона в Мічиганському університеті. Пізніше він зацікавився науковою статтею 1983 року у журналі Science, яка стверджувала, що у Північній Каліфорнії почали госпіталізувати молодих людей із раптовою хворобою Паркінсона. Всі ці молоді люди вживали наркотик із хімічною сполукою MPTP. Вона руйнує нейрони чорної субстанції, пошкоджуючи в них роботу мітохондрій — структур, які забезпечують клітини енергією. Але Грінамайр знав, що MPTP не єдиний має таку дію, серед них — поширений рослинний пестицид ротенон.
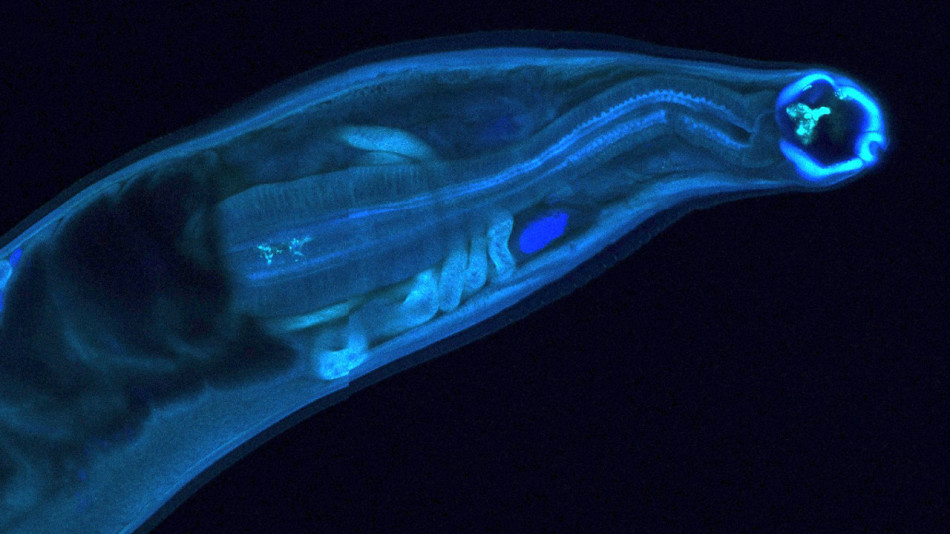
До 2000 року Тіму та його команді стало зрозуміло, що ротенон спричиняє у пацюків руйнування тих самих нейронів чорної субстанції, що уражаються й у людей при хворобі Паркінсона. Так само, у нейронах, що вижили, він призводить до накопичення фібрилярного білка, схильного до скупчення. У такій формі він сильно нагадував тільця Леві — внутрішньоклітинні структури, які є однією з основних діагностичних рис хвороби Паркінсона. Поведінка тварин теж підозріло нагадувала недугу — вони мали нестійку поставу та непевні рухи, а також тремор кінцівок.

Оксидативне пошкодження (пурпурний) дофамінергічного нейрона пацюка (синій) після обробки пестицидом ротеноном. MATTHEW T. KEENEY / UNIVERSITY OF PITTSBURGH
Цим відкриттям науковці показали дві важливі речі — що у добре вивчених лабораторних тварин можна спричинити прояви хвороби Паркінсона, дозволивши дослідження на них цієї недуги, і що інші пестициди, можливо, теж володіють подібною токсичною дією.
Боротьба зі шкідниками
Зараз Грінамайр міркує, чи міг ротенон та подібні до нього сполуки стати причиною його хвороби. Перш ніж ввести його гризунам та спричинити цим у них прояви хвороби Паркінсона, ротенон слід розчинити у диметилсульфоксиді. Час від часу цей розчин потрапляв на рукавиці Тіма, а через них — у шкіру. У той час він і його колеги не усвідомлювали можливу небезпеку контакту з ротеноном, однак одне з досліджень 2011 року вказало, що у фермерів, які користуються цим пестицидом, та у їхніх дружин і чоловіків ризик розвитку хвороби Паркінсона підвищений у 2,5 раза.
Робота Грінамайра із токсинами також посприяла оформленню позову на Агенство з охорони навколишнього середовища США (EPA), яке 2021 повторно схвалило гербіцид паракват. Ця речовина, якою дозволили труїти бур'яни, викликає у гризунів ознаки хвороби Паркінсона, подібно до ротенону. У деяких лабораторіях її навіть використовували для створення тваринних моделей хвороби, навмисно піддаючи пацюків параквату.
Між тим, EPA казало, що можлива користь від його використання у сільському господарстві переважує імовірну шкоду людському здоров'ю. Грінамайр як незалежний експерт тоді вказав на те, що агенство нехтує численними науковими дослідженнями, які свідчать про ризики параквату, який заборонений щонайменше у 50 країнах світу. Хоч EPA зрештою залишилися при думці, що наразі немає достатньо даних про зв'язок параквату й ротенону при звичайному використанні із хворобою Паркіонсона, інші нейронауковці вважають аргументи Тіма переконливим та важливим внеском у справу.
Погані гени
Але річ не лише у можливих токсинах. Дослідники припускають, що основна причина хвороби Паркінсона лежить у генах. Всупереч тому, що у 90 відсотках випадків неможливо встановити точну причину захворювання, найімовірніше, що за ним стоїть поєднання генетичної схильності та фактора довкілля, який її активував. Зокрема, на це вказує руде волосся — у людей із генами такого кольору волосся, яким у молодості міг похизуватися і Грінамайр, ризик хвороби Паркінсона вищий, ніж в інших.
Та в інших 10 відсотках випадків хвороба Паркінсона явно спричинена генетичним дефектом. 1997 року вчені виявили першу таку мутацію. Вона відповідає за вироблення білка альфасинуклеїну. Невдовзі список розширився до гена білка Паркін, а також ферментів LRRK2 та глюкоцереброзідаза.
Ці разючі відкриття у сфері інтересів Грінамайра пройшли на фоні його болючої особистої драми. Важке розлучення змусило його переїхати до нового міста у 2004 році. Також він зіткнувся із браком фінансування. Але всупереч усьому він залишився вірним своїй праці, та зосередився на пошуках відповідей щодо механізму впливу гена LRRK2, мутації якого відповідальні за приблизно 3-4 відсотки випадків хвороби Паркінсона.
Фермент, що кодується геном LRRK2, є регулювальником руху білків та везикул всередині клітин. Окремі мутовані варіанти роблять його надмірно активним, через що пошкоджується функція лізосом — клітинних органел-везикул, які розщеплюють вже непотрібні білки та клітинні структури. Внаслідок цього у нейронах накопичуються відходи, зокрема патологічний альфа-синуклеїн, що порушує нормальну роботу дофамінових нейронів.

1 — Альфа-синуклеїн. Через неправильне згортання цей білок токсичний і схильний накопичуватися у нейронах. Антитіла, вакцини та малі молекули, такі як UCB0599, спрямовані на запобігання або відвернення цього. 2 — Глюкоцереброзидаза. Пригнічена активність цього ферменту при хворобі Паркінсона пов’язана з накопиченням токсичного альфа-синуклеїну. Дослідники намагаються відновити його активність за допомогою генної терапії та таких препаратів, як амброксол, що початково призначений для лікування кашлю. 3 — LRRK2. Цей фермент є надмірно активним у деяких пацієнтів, що, ймовірно, спричиняє пошкодження лізосом, накопичення токсичних побічних продуктів у клітинах і нейродегенерацію. Деякі ліки та синтетичні генетичні фрагменти, які називаються антисмисловими олігонуклеотидами, спрямовані на придушення активності LRRK2.
Але дослідження Грінамайра у 2021 році показали, що є токсична сполука, здатна зімітувати мутацію LRRK2. Розчинник трихлоретилен, що його використовують у хімчистці та для знежирення металу, спричиняв у його старих лабораторних пацюків патологію, як при хворобі Паркінсона, посилюючи активність гена LRRK2. Це відкриття лягло в основу позову людей, які десятиліття тому споживали забруднену трихлоретиленом воду на базі Корпусу морської піхоти у Північній Кароліні, та які стверджували, що сполука спричинила у них хворобу Паркінсона.
Наступні вивчення Грінамайра вказали, що навіть у людей із хворобою Паркінсона без мутації експресія гена LRRK2 збільшена. Коли науковці дали сполуку, яка пригнічує LRRK2, мишам після ротенону, це усунуло негативний вплив пестициду та не дало розвиватися проявам хвороби Паркінсона. Тоді з'явилася думка, що блокуванням LRRK2 можна лікувати хворобу і в людей. І зараз компанія Biogen тестує таке лікування на тисячі добровольців із хворобою Паркінсона, прагнучи спинити прогресування захворювання.
Відповіді за горизонтом
Коли близький друг Тіма і лікар підтвердив хворобу Паркінсона у колеги, то відмітив, що Грінамайр сприйняв новину з гідністю та апломбом. Дослідник почав лікування леводопою, яку до того сам численні рази призначав своїм пацієнтам, і його симптоми помалу зменшилися.
Водночас Тім зізнається, що іноді, як і його пацієнти, він тривожиться, коли помічає незвичайні відчуття у тілі — можливо, це поколювання теж є проявом хвороби? Але разом із тим він оптимістично налаштований щодо перспектив у лікуванні хвороби Паркінсона. На його думку, наука вже наблизилася до суті проблеми, хоч відповіді поки що знаходяться за горизонтом.