Навіть для сучасної науки рак підшлункової залози залишається одним із найагресивнішим і найстійкіших до лікування, але нещодавно команда іспанських науковців подарувала нову надію у боротьбі з цією недугою. Дослідники повністю подолали рак підшлункової в мишей — без агресивної хімієтерапії чи опромінення, лише завдяки комбінації трьох націлених на пухлини препаратів. Однак між успішним експериментом на мишах і появою нового стандарту лікування для людей лежить довгий і складний шлях.
Що робить лікування раку підшлункової залози одним із найскладніших завдань для медиків і який прогрес зробили в ньому іспанські дослідники? Чому результат можна вважати обнадійливим, але поки що не революційним? Розбираємося в питанні з самих основ разом із Ростиславом Лозинським, кандидатом медичних наук (Німеччина).
Цей матеріал першими прочитали учасники нашої спільноти — саме завдяки їхнім донатам nauka.ua може замовляти такі експертні розбори. Приєднуйтесь — підтримаєте науковий контент українською і читатимете нові матеріали раніше за всіх.
Що прийшло на заміну хімієтерапії?
Сучасне лікування злоякісних пухлин дуже сильно відрізняється від методів XX століття, які базувалися на використанні хімієтерапії — препаратів, що шкодять не лише раковим клітинам, а й здоровим. Тепер завдяки генетичним дослідженням зрозуміло, що в основі більшості відомих пухлин лежать шкідливі зміни в конкретних генах, які запускають некероване розмноження ракових клітин. Знешкоджувати самі гени поки не дуже вміють, а от прицільно зупинити роботу шкідливого білка, який клітина створила за інструкцією ракового гена — онкогена — вже іноді вдається.
Пошук таких препаратів — кропітка справа, але вже існують сотні випробуваних ліків із таким механізмом дії. Вони зв'язуються з конкретним хвороботворним білком — тому називаються прицільними, або таргетними. Такі ліки є проти лейкемії, раку грудей, раку прямої кишки, легень та інших. Вони поки що дорогі, але нерідко значно дієвіші за інші: люди, яким лишалися лічені місяці, завдяки таргетній терапії живуть роками, іноді — десятиліттями. Наприклад, один з перших таких препаратів — іматиніб — дозволив ще у середині 2010-х збільшити тривалість життя хворих на хронічну мієлоїдну лейкемію, одного зі злоякісних новоутворень крові, на понад десятиліття.
І здавалося б, що ідеальне лікування вже знайдено. Але, на жаль, це не зовсім так, оскільки навіть прицільні препарати не завжди можуть впоратися з агресивним раком.
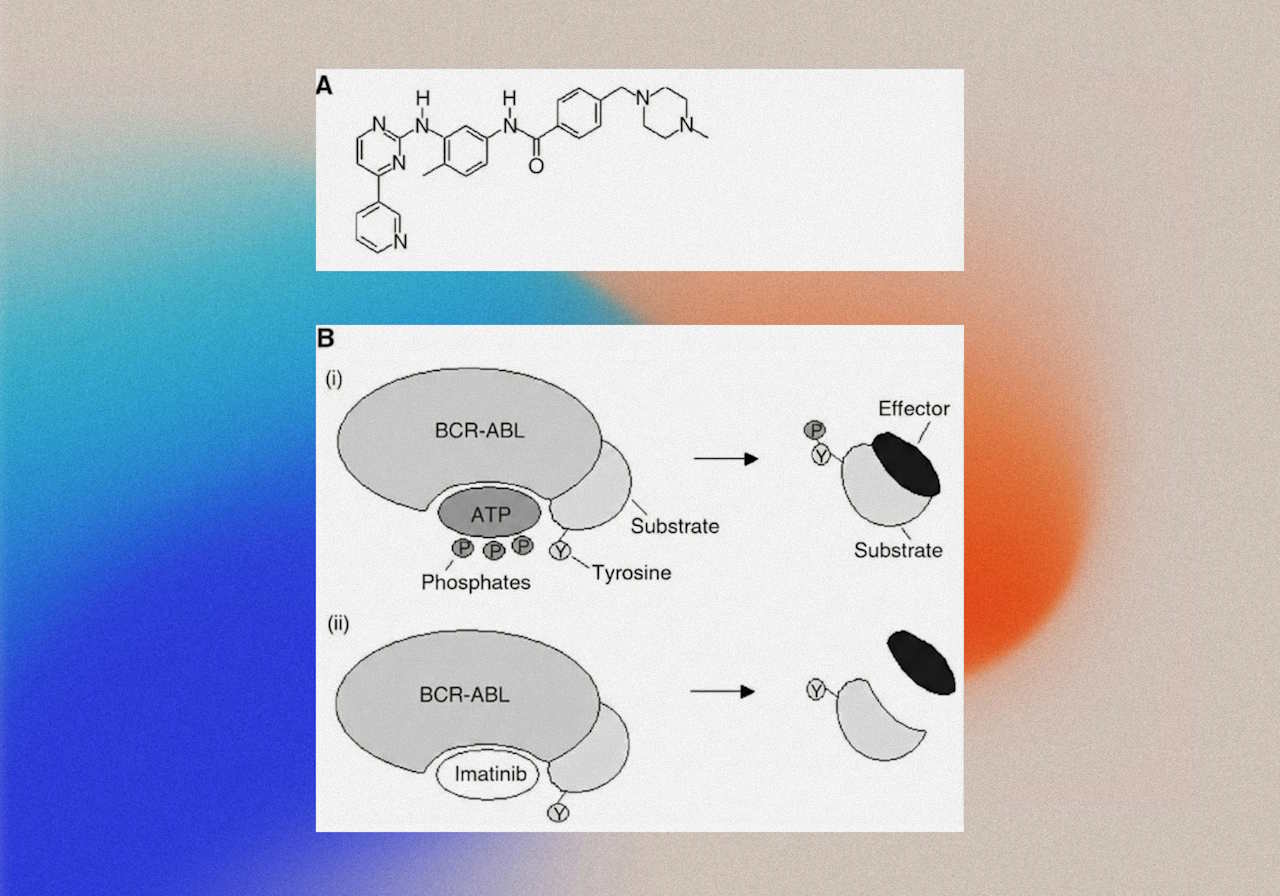
У чому слабкість прицільних препаратів?
Для багатьох пухлин прицільні препарати або не працюють зовсім, або до них дуже швидко виникає стійкість. Причина в тому, що клітини — зокрема пухлинні — це складні білкові машини, де багато процесів, особливо таких важливих як ріст і розмноження, багаторазово дублюються.
У раковій пухлині не всі клітини однакові: багато з них мають свої особливості, сильні та слабкі сторони. Знищення хворих клітин нагадує боротьбу з армією, яка має безліч способів ухилитися від удару, «окопатися» в непрохідних лініях оборони, наставити системи ППО і пристосуватися з часом до кожної нової тактики.
Щоб подолати ці «лінії оборони», одного препарату буває замало. Можна використати кілька ліків, які впливають на різні ланки життєдіяльності пухлин, або збільшити дозу. Проте значне збільшення дози дуже часто призводить до наростання побічних ефектів — іноді смертельно небезпечних, з відмовою печінки, нирок чи серця.
Інший ризик ховається в небажаних діях ліків. Логічно було б очікувати, що прицільні препарати не спричинятимуть побічних ефектів, адже діють лише проти конкретних генетичних поломок, але реальність виявилася іншою. Той самий іматиніб, який начебто дуже прицільно діє при хронічній мієлоїдній лейкемії, як з'ясувалося, допомагає і при зовсім інших захворюваннях — пухлині шлунково-кишкового тракту та гіпереозинофільних синдромах, які є порушенням роботи імунної системи. З одного боку — одні ліки від кількох серйозних хвороб. З іншого — це означає, що препарат діє не лише на єдину специфічну мішень, а впливає й на інші процеси, які не завжди зрозумілі, і не завжди — на краще. Дослідження експресії генів при додаванні іматинібу показало чимало змін поза його основною мішенню — патологічним білком гена BCR/ABL. А пацієнти і їхні лікарі добре знають, що приціл у сучасних таргетних препаратів не завжди точний, і побічних ефектів — чимало.
Чому рак підшлункової такий складний для лікування?
Іматиніб — це все одно історія великого успіху, попри обмеження. У багатьох інших таргетних препаратів ефект далеко не такий разючий. Наприклад, при раку легень із мутацією в гені рецепторів епідермального фактора росту (EGFR) допомагає препарат афатиніб, який блокує білки цих рецепторів. Клінічні дослідження показали, що афатиніб у комбінації з хімієпрепаратом пеметрекседом може збільшити виживання без прогресування пухлини з 6,9 до 11,1 місяця порівняно з «чистою» хімієтерапією цисплатином та пеметрекседом.
Оскільки білки EGFR надмірно утворюються в багатьох пухлинах і афатиніб відносно добре сприймається організмом, з'явилися ідеї використати його й при інших видах раку. Зокрема, при раку підшлункової залози — особливо агресивному й стійкому до звичайної хімієтерапії. Шанси на п'ятирічне виживання при цьому раку становлять у середньому лише близько п'яти відсотків, а за наявності метастазів — ще менше.
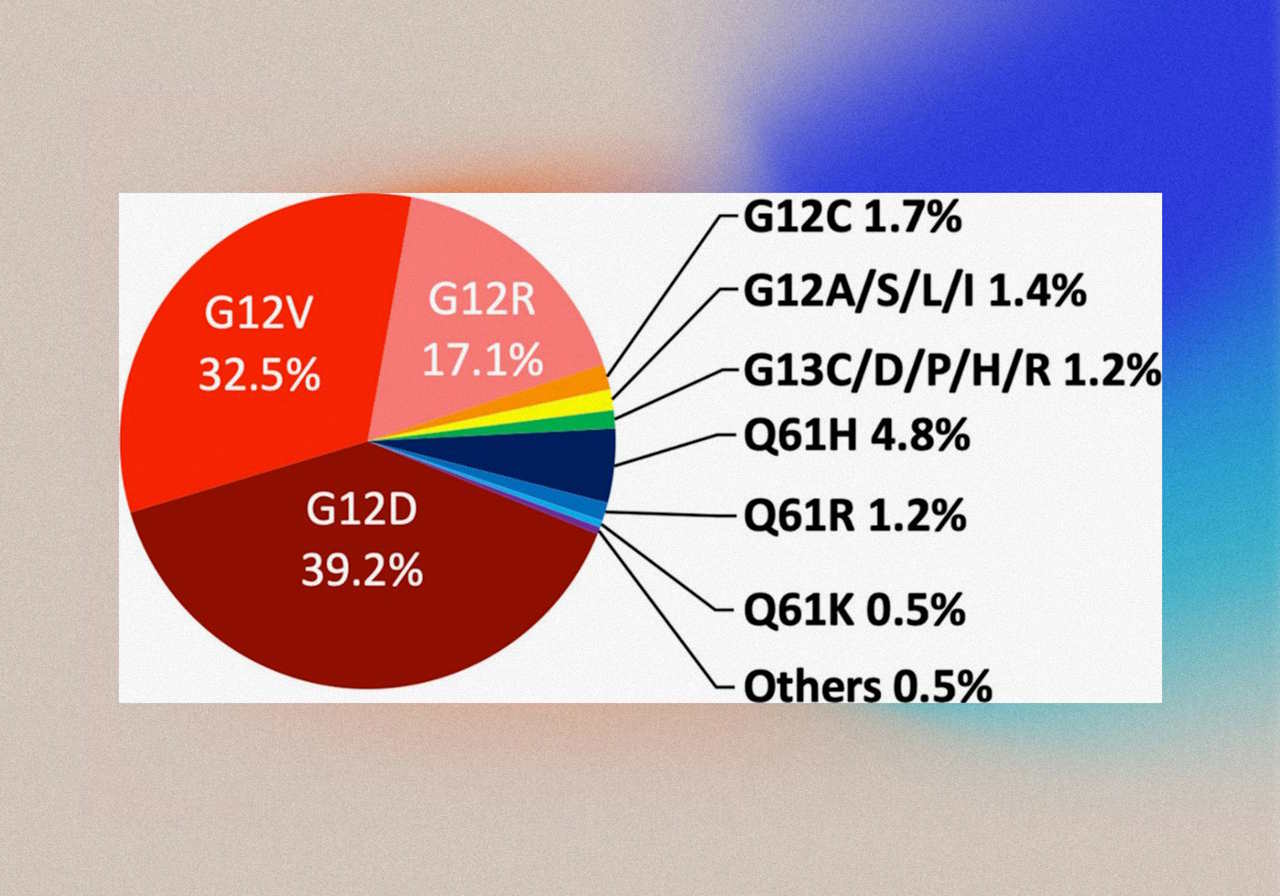
Водночас у близько 85 відсотків хворих на рак підшлункової залози виявляють мутації й у гені KRAS. Прицільних препаратів проти мутацій цього гена поки обмаль. Розробку ускладнює те, що в одному гені трапляється багато різних мутацій, а створювати ліки проти кожної окремо — дорого й малоефективно. Тому наразі немає клінічно перевірених препаратів проти найпоширеніших мутацій при раку підшлункової: KRAS G12D і KRAS G12V.
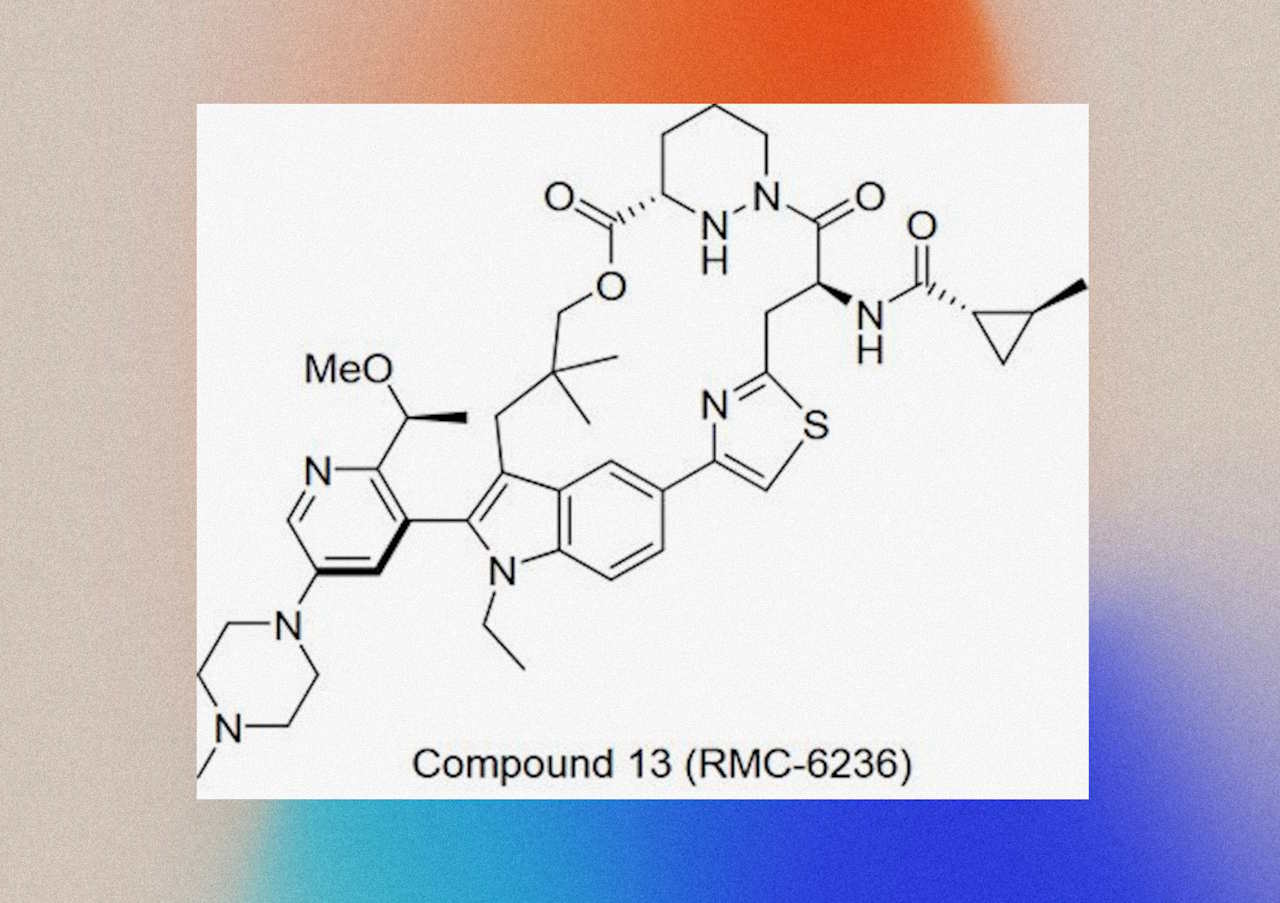
Попри це, дослідники не полишають спроб знайти універсальний препарат, який блокуватиме всі або хоча б більшість варіантів хвороботворних білків цього гена. Зараз тривають великі міжнародні дослідження на великій кількості пацієнтів пан-KRAS-інгібітора дараксонрасибу. Проблема лише в тому, що для раку легень із такими ж мутаціями цей препарат виявився лише обмежено ефективним: об'єктивне клінічне покращення отримали у 38 відсотків хворих, причому в понад 90 відсотків пацієнтів спостерігалися побічні ефекти різної інтенсивності.
Як підійшли до проблеми раку підшлункової іспанські дослідники?
Коли препарат сам по собі діє недостатньо, а збільшення дози лише додає побічних ефектів — чи не варто спробувати комбінацію? Саме це й зробила іспанська команда з Національного центру онкологічних досліджень у Мадриді, з групи Маріано Барбасіда (Mariano Barbacid) — одного з першовідкривачів ролі мутацій генів групи Ras в онкології. Дослідники поєднали три прицільні препарати: дараксонрасиб та афатиніб, кожен із яких діє на різні ланки роботи пухлинної клітини — KRAS та EGFR, з експериментальним препаратом SD-36, який запускає руйнування білка STAT3, важливого в розмноженні ракових клітин.
Як розповіли науковці у своїй статті в журналі Proceedings of the National Academy of Sciences, таке поєднання змогло знищити штучно викликаний варіант раку підшлункової залози в мишей, а самі тварини прожили 200-300 днів без повернення пухлин. Дієвим лікування виявилося й проти людських ракових клітин, пересаджених мишам.
Та важливо зазначити, що комбінація кількох ліків — не нова стратегія. Одночасне поєднання препаратів не завжди дієвіше, зате часто — значно токсичніше. Наприклад, дослідження одночасного застосування афатинібу з хімієпрепаратом гемцитабіном для лікування раку підшлункової не показало жодного покращення виживання порівняно з самою хімієтерапією — пацієнти прожили трохи більш як сім місяців). Натомість різко зросла кількість побічних ефектів: зокрема, діарея виникла у 71 відсотка хворих від комбінації проти 13 відсотків від самої лише хімієтерапії, шкірний висип — у 65 відсотків проти п'яти. Наразі для людей не знайшли жодної безпечної комбінації з афатинібом.
Обнадійливі результати іспанської групи дослідження раку підшлункової залози на мишах вказують на те, що, скоріше всього, обмін цього препарату в мишей відбувається інакше, ніж у людей. Науковці використовували дозу 20 міліграмів на кілограм маси тварин, тоді як у людей призначають близько 0,5 міліграмів на кілограм — у 40 разів менше. Так само дослідники використали суттєво більші дози дараксонрасибу, ніж у клінічних дослідженнях на людях, — при тому, що навіть у нижчих дозах цей препарат викликає помітні побічні ефекти. Доза, яку добре переносить миша, може просто вбити людину.
Такі відмінності обміну речовин між різними ссавцями — не дивина, але вони дуже ускладнюють пошук ефективних ліків. Мишачі моделі не завжди відображають те, що відбуватиметься в людей. Десятки, навіть сотні препаратів, які успішно випробували на мишах чи пацюках, не працюють у людей. Іноді причина — у відмінностях між видами, іноді — у недосконалості клітинних культур, які вводять дослідним мишам: ці культури можуть походити зі справжньої пухлини, але все одно не є стовідсотковим відповідником пухлинного процесу в живих людей.
Який тоді сенс вивчати рак на мишах?
Ідеального модельного організму, дані з якого можна з високою ймовірністю перенести на людей, наразі не існує. Але це не означає, що досліджувати не потрібно. Миші — далекі від людини за багатьма показниками, проте вони маленькі, швидко розмножуються і їх відносно просто утримувати. Про біологію мишей відомо, мабуть, більше, ніж про біологію людини. І кожен успіх у лікуванні пухлин у мишей наближає ефективніше лікування для людей. Усі сучасні прицільні препарати в певний момент тестували на мишах — без цих дослідів не було б мільйонів врятованих життів.
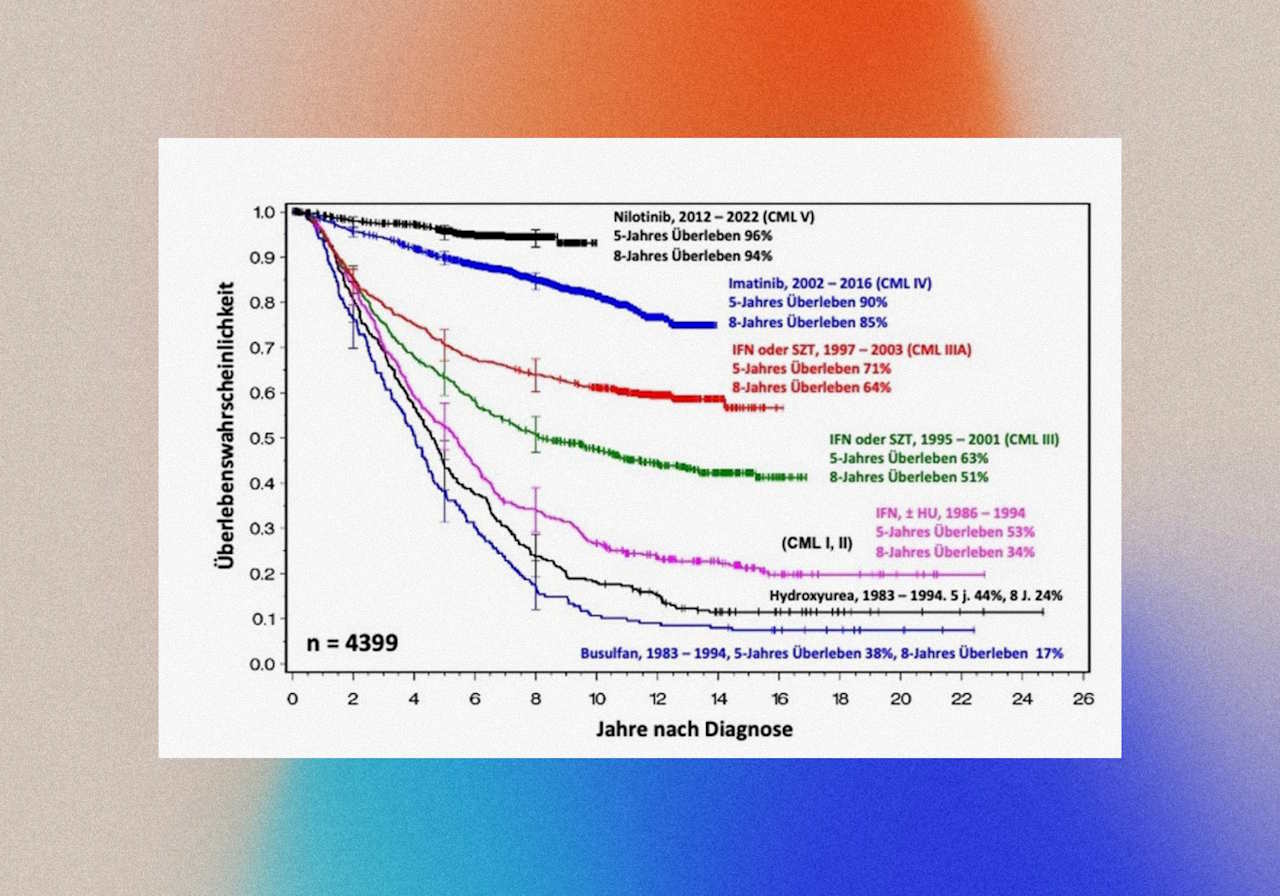
Дослідження потрійної комбінації таргетних ліків для раку підшлункової залози, попри нереальність прямого застосування саме такої комбінації в людей, показує принципову можливість: знищити агресивну пухлину без хімієтерапії, без опромінення, без важких операцій — лише завдяки блокуванню конкретних клітинних білків. Прогрес у цій сфері не стоїть на місці. Замість афатинібу вже з'явився значно «прицільніший» озимертиніб; замість іматинібу новим «золотим стандартом» став нілотиніб, який ще більше подовжує життя хворих, точніше зв'язуючись зі своєю мішенню. Прогрес у розумінні та лікуванні раку за останні роки — надзвичайний.
Це дає надію на те, що рак підшлункової залози з часом теж стане або виліковним, або хоча б так добре контрольованим, як хронічна мієлоїдна лейкемія. Але між мишачими результатами й реальними ліками — роки клінічних випробувань, пошуку безпечних доз і подолання резистентності.